ハンチントン病のいくつかの機能は、次の方法で管理できます。
- 言語療法、心理療法、認知リハビリテーションは、病気の身体的症状と心理的症状の両方を改善することができます。特に、これらの治療法は、コミュニケーションや日常の活動の自律的な実行を支援するのに役立ちます。行動障害と認知障害をよりよく理解することは、ハンチントン病の進行によって引き起こされる変化に適応するための戦略を開発するのにも役立ちます。
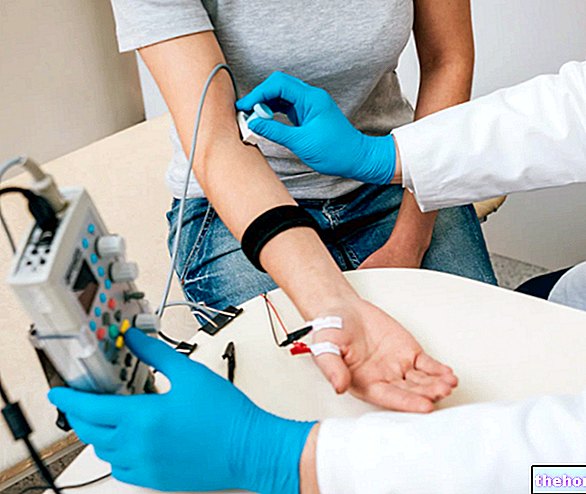
- 理学療法と定期的な運動:運動協調性の維持に貢献します。病気の初期段階では、穏やかな身体活動(水泳、ウォーキングなど)が推奨されます。
- 協調運動障害を経験しているハンチントン病患者が自立して歩くのを助けるための特定の補助具の使用。
- 薬:重要な症状が発生したときに適応されます。たとえば、ドーパミン受容体を遮断または枯渇させる薬で舞踏病や興奮を部分的に抑えることができますが、多くの薬は副作用を引き起こすだけでなく、患者ごとに異なる効果をもたらす可能性があるため、薬物療法の理想的なバランスを確立する必要があります症状と治療に対する個々の反応に基づいて、専門の医師によってケースバイケースで。
、ハンチントン病の治療に。臨床段階は非常に厳しいものです。主な理由は、この病気の進行が遅く、「臨床の不均一性が広いためです。ハンチントン病の評価の尺度はあり、すべての診療所でほぼ同じです。病気の完全な浸透度と利用可能性テスト。予測遺伝学、それは病気の初期段階の間に治療を試みる機会を提供します。現在、これらの研究は、疾患の最初の症状に介入するために、変化の敏感で安定したバイオマーカーの検索を目的としています。
現在、ニューロイメージング技術は、前駆期(疾患の臨床症状に先行する)の間に最高のバイオマーカーを提供しています。さらに、それらは動物モデルと人間に対して行われた治療の間の相関関係を提供します。
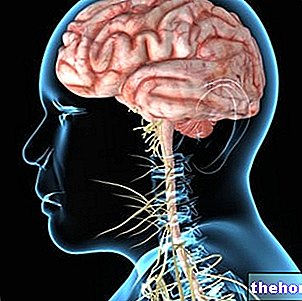
前述のように、線条体の萎縮は初期であり、病気の経過中に進行します。皮質下および皮質の白質構造などの脳の他の領域も、前駆期に影響を受けることが示されています。
機能イメージングを通じて、前駆期の個人の特定の異常を特定することもできます。この手法は、検出可能な構造の不規則性や行動の変化を特定するのに十分な感度もあります。
最後に、乳酸や他の細胞ストレス産物などの分子バイオマーカーの同定は、磁気共鳴分光法のおかげで可能になります。
ハンチントン病におけるニューロンの選択的変性はまだ完全には解明されていません。したがって、可能な新しい治療戦略を調査する必要があります。特に、ハンチントン病では、大脳基底核のCB1型カンナビノイド受容体が選択的に失われることがわかっています。これは、最も初期の神経化学的変化の1つです。このため、研究研究は現在、ハンチントン病におけるカンナビノイドの神経保護的役割を調査しています。
詳細情報:カンナビノイド受容体ハンチントン病:CB1受容体
ハンチントン病における内在性カンナビノイドシステム、特にCB1受容体の関与は長い間仮説が立てられてきました。確かに、この病気に冒された個人の最初の明らかな変化の1つは、基底核のCB1受容体の選択的喪失であることが示されています。この受容体喪失は、線条体神経病理の発症に先行します。ハンチントン病のトランスジェニック動物モデルでは、 CB1受容体発現と内在性カンナビノイドレベルの両方の変化が観察されました。これらの証拠は、内在性カンナビノイドシステムの調節不全が新しい治療戦略の開発の標的となる可能性があるという仮説を導きました。
ごく最近の研究では、ハンチントン病のトランスジェニックモデルにおけるCB1受容体の欠失が、大麻アゴニストによる慢性治療中に、「線条体萎縮およびハンチンチンタンパク質の蓄積」において運動表現型の悪化をもたらしたことが示されています。 、テトラヒドロカンナビノール(Δ9-THC)は有益でした。
最後に、CB1受容体は、前の段落で説明したように、ハンチントン病の影響を受ける脳領域である線条体のニューロンの90〜95%を構成するGABA作動性ニューロンで高度に発現しています。
CB1受容体の刺激は、抑制性神経伝達物質GABAの放出の減少につながります。この減少は、GABAによって発揮される抑制性緊張を減少させることによって、グルタミン酸によって決定される興奮性緊張が過度に増加し、その結果、興奮毒性の現象が生じることを考えると、ハンチントン病に冒された患者にとって有害である可能性があります。興奮毒性は、線条体の投射ニューロンの死に寄与すると考えられていますが、CB1受容体は、程度は低いものの、グルタメートニューロンにも存在します。これらの受容体の刺激は、グルタメートの放出の低下にもつながるとの仮説が立てられています。 Δ9-THCによる慢性治療が有益であったという事実は、特定のニューロンにおけるカンナビノイドアゴニストへの応答の媒介におけるCB1受容体の寄与が疾患の進行において変化する可能性があることを示唆しています。
今後の展望
現在、ハンチントン病の治療法の探索が活発であり、ハンチンチンの産生を減らすことができるさまざまな薬理学的薬剤および/または非薬理学的アプローチ(例えば、遺伝子治療、幹細胞移植)の有効性を評価するためのいくつかの臨床試験が進行中です。またはニューロンの生存を改善し、病気の進行を予防または遅らせます。
たとえば、RNA干渉(RNAi)またはアンチセンスオリゴヌクレオチド(ASO)を使用した遺伝子サイレンシング。 ASOは、特に、変異した遺伝子からの「情報を運ぶメッセンジャーRNA」に結合し、その翻訳をブロックし、その分解を刺激して、ハンチンチンタンパク質が生成されないようにします。一方、幹細胞治療は、脳の患部に幹細胞を移植することで、損傷したニューロンを置き換えることから成ります。動物モデルと予備臨床試験での試験は、この技術と矛盾する結果をもたらしたので、その有効性を確立するためにさらなる証拠が必要です。
参考文献
- キャロン、N.S。、ライト、G.E.B。 &Hayden、M.R。ハンチントン病。 GeneReviews((R))ハンチントン病。シアトル(WA)、2018年。
- NeurobiolDis。 2012年3月; 45:983-91。土井:10.1016 /j.nbd.2011.12.017。 Epub 2011 12月23日。ハンチントン病のトランスジェニックマウスモデルのGABA作動性およびグルタミン酸作動性ニューロンで発現するCB1受容体の不均衡。ChiodiV、Uchigashima M、Beggiato S、Ferrante A、Armida M、Martire A、Potenza RL、Ferraro L、 Tanganelli S、Watanabe M、Domenici MR、PopoliP。




















.jpg)




