有効成分:ミラベグロン
Betmiga 25mg徐放錠
Betmiga 50mg徐放錠
Betmigaが使用されるのはなぜですか?それはなんのためですか?
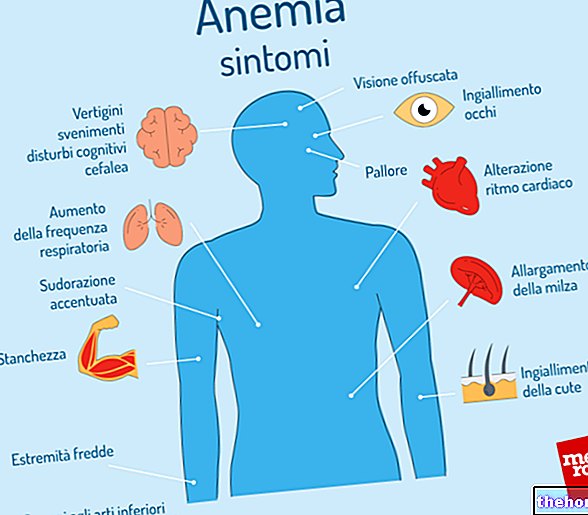
Betmigaには有効成分のミラベグロンが含まれています。これは膀胱筋弛緩薬(いわゆるベータ3アドレナリン受容体アゴニスト)であり、過活動膀胱の活動を低下させ、その症状を治療します。
Betmigaは、次のような成人の過活動膀胱症候群の症状を治療するために使用されます。
- 膀胱を空にする突然の必要性(いわゆる緊急性)
- 通常よりも頻繁に膀胱を空にする必要性(いわゆる頻尿)
- 膀胱が空になるのを制御できない(いわゆる切迫性尿失禁)。
Betmigaを使用すべきでない場合の禁忌
Betmigaを服用しないでください:
- ミラベグロンまたはこの薬の他の成分のいずれかにアレルギーがある場合(セクション6に記載)。
- あなたが制御できない非常に高い血圧を持っているならば。
使用上の注意Betmigaを服用する前に知っておくべきこと
Betmigaを使用する前に、医師または薬剤師に相談してください。
- 膀胱を空にするのに問題がある場合、尿の流れが弱い場合、または過活動膀胱のために抗ムスカリン薬などの他の薬を服用している場合
- 腎臓や肝臓に問題がある場合。特にイトラコナゾール、ケトコナゾール、リトナビル、クラリスロマイシンなどの他の薬を服用している場合は、医師が用量を減らす必要があるか、ベトミガを使用しないように指示することがあります。他の薬を服用している場合は、医師に相談してください。
- あなたが非常に高い制御されていない血圧を持っている場合。
- QT延長として知られる「ECG異常」(心臓活動の追跡)がある場合、またはこの異常を引き起こすことが知られている薬を服用している場合:キニジン、ソタロール、プロカインアミド、イブチリドなどの心臓リズム障害の治療に使用される薬、フレカイニド、ドフェチリド、アミオダロン、アレルギー性鼻炎の治療に使用される薬剤、チオリダジン、メソリダジン、ハロペリドール、クロルプロマジンなどの抗精神病薬(精神疾患の治療に使用される薬剤)、ペンタミジン、モキシフロキサシン、エリスロマイシンなどの抗感染薬。
高血圧を経験した場合、ミラベグロンは血圧を上昇または悪化させる可能性があります。ミラベグロンを服用している間は、医師が血圧をチェックすることをお勧めします。
子供と青年
この年齢層でのベトミガの安全性と有効性はまだ実証されていないため、18歳未満の子供や青年にこの薬を投与しないでください。
相互作用どの薬や食品がベトミガの効果を変えることができるか
他の薬を使用している、最近使用した、または使用する可能性があるかどうかを医師または薬剤師に伝えてください。
Betmigaは他のいくつかの薬の働きに影響を与える可能性があり、他のいくつかの薬はBetmigaの働きに影響を与える可能性があります。
- チオリダジン(精神疾患の治療に使用される薬)、プロパフェノンまたはフレカイニド(心調律障害の治療に使用される薬)、イミプラミンまたはデシプラミン(うつ病の治療に使用される薬)を服用しているかどうかを医師に伝えてください。これらの特定の薬はあなたの医者があなたの用量を調整することを要求するかもしれません。
- 心不全や不整脈の治療に使用される薬であるジゴキシンを服用しているかどうかを医師に伝えてください。この薬の血中濃度は医師が測定します。血中濃度が異常な場合は、医師がジゴキシンの投与量を調整することをお勧めします。 。
- ダビガトランエテキシレート(不整脈(心房細動)やその他の要因のリスクがある成人患者の血栓形成によって引き起こされる脳または体の血管の閉塞のリスクを軽減するために使用される薬)を服用しているかどうかを医師に伝えてください。この薬はあなたの医者による用量調整を必要とするかもしれません。
警告次のことを知っておくことが重要です。
妊娠と母乳育児
妊娠している場合は、妊娠している可能性がある、または妊娠を計画していると考えて、Betmigaを使用しないでください。
授乳中の方は、この薬を使用する前に医師または薬剤師に相談してください。この薬は母乳に移行する可能性があります。医師と一緒に、ベトミガと母乳のどちらを服用するかを決める必要があります。両方を行うことはできません。
機械の運転と使用
この薬が機械を運転または使用する能力を損なうことを示す利用可能なデータはありません。
投与量、投与方法および投与時間Betmigaの使用方法:Posology
常に医師の指示どおりに使用してください。疑わしい場合は、医師または薬剤師に相談してください。
推奨用量は、1日1回経口摂取される50mgの錠剤1錠です。腎臓や肝臓に問題がある場合は、医師が1日1回経口摂取する25mg錠1錠に減量する必要があるかもしれません。この薬を液体と一緒に服用し、錠剤全体を飲み込んでください。タブレットを壊したり噛んだりしないでください。 Betmigaは、食事の前、最中、または後に服用できます。
過剰摂取ベトミガを飲みすぎた場合の対処方法
必要以上にベトミガを服用した場合
処方された量よりも多くの錠剤を服用した場合、または他の誰かが誤って錠剤を服用した場合は、すぐに医師、薬剤師、または病院に連絡してください。
過剰摂取の症状には、頻脈、脈拍の増加、血圧の上昇などがあります。
Betmigaを服用するのを忘れた場合
飲み忘れた場合は、次の服用まで6時間以内の場合を除き、覚えたらすぐに飲んでください。その後、通常の時間に薬を服用し続けます。
忘れた分を補うために2回分を服用しないでください。飲み忘れた場合は、医師に連絡し、アドバイスに従ってください。
Betmigaの服用をやめた場合
すぐに効果が見られない場合は、Betmigaの服用を時期尚早に中止しないでください。膀胱の調整には時間がかかる場合があります。錠剤を服用し続けてください。
膀胱の状態が改善したときに治療を中止しないでください。治療を中止すると、過活動膀胱症候群の症状が再発する可能性があります。過活動膀胱症候群の症状が再発する可能性があるため、最初に医師に相談せずにベトミガの服用を中止しないでください。
この薬の使用についてさらに質問がある場合は、医師または薬剤師に相談してください。
副作用ベトミガの副作用は何ですか
すべての薬と同様に、この薬は副作用を引き起こす可能性がありますが、誰もがそれらを得るわけではありません。
最も深刻な副作用には、不整脈(心房細動)が含まれる場合があります。これはまれな副作用です(100人に1人まで影響する可能性があります)が、この副作用が発生した場合は、薬の服用を中止し、すぐに医師に相談してください。
その他の副作用は次のとおりです。
一般的な副作用(10人に1人まで影響を受ける可能性があります)
- より速い心拍数(頻脈)
- 尿を運ぶチャネルの感染症(尿路感染症)-吐き気
まれな副作用(100人に1人まで影響を受ける可能性があります)
- 膀胱感染症(膀胱炎)
- 心拍の認識(動悸)
- 膣感染症
- 消化不良(消化不良)
- 胃の感染症(胃炎)
- 関節の腫れ
- 外陰部または膣のかゆみ(外陰膣のかゆみ)
- 血圧の上昇
- 肝酵素の増加(GGT、AST、ALT)
- かゆみ、発疹または発疹(じんましん、発疹、斑状丘疹、丘疹性発疹、そう痒症)
まれな副作用(1,000人に1人まで影響する可能性があります)
- まぶたの腫れ(まぶた浮腫)
- 唇の腫れ(唇の浮腫)
- 顔、舌、喉などの体のあらゆる部分に影響を及ぼし、呼吸困難を引き起こす可能性のある水分の増加によって引き起こされる、皮膚のより深い層の腫れ。
- 小さな紫がかった皮膚の発疹(紫斑)
- 主に皮膚に影響を与える小血管の炎症(白血球破砕性血管炎)
- 膀胱を完全に空にすることができない(尿閉)
不明(利用可能なデータから頻度を推定することはできません)
- 不眠症
Betmigaは、膀胱閉塞がある場合、または過活動膀胱を治療するために他の薬を服用している場合、膀胱を空にするのをより困難にする可能性があります。膀胱を空にできない場合は、すぐに医師に連絡してください。
副作用の報告
副作用が出た場合は、医師または薬剤師に相談してください。これには、このリーフレットに記載されていない可能性のある副作用も含まれます。付録Vに記載されている国の報告システムを介して直接副作用を報告することもできます。副作用を報告することにより、この薬の安全性に関するより多くの情報を提供するのに役立ちます。
有効期限と保持
この薬は子供の視界や手の届かないところに保管してください。
EXP後のカートン、ブリスター、ボトルに記載されている有効期限後は、この薬を使用しないでください。有効期限は、その月の最終日を指します。
この薬は特別な保管条件を必要としません。
最初にボトルを開けた後、錠剤は6ヶ月以内に使用する必要があります。
廃水や家庭ごみで薬を捨てないでください。使用しなくなった薬は薬剤師に捨ててください。環境保護に役立ちます。
組成および剤形
Betmigaに含まれるもの
- 有効成分はミラベグロンです。各錠剤には、25mgまたは50mgのミラベグロンが含まれています。
- その他の成分は次のとおりです。錠剤コア:マクロゴール、ヒドロキシプロピルセルロース、ブチルヒドロキシトルエン、ステアリン酸マグネシウム。コーティング:ヒプロメロース、マクロゴール、黄色酸化鉄(E172)、赤色酸化鉄(E172)(25 mg錠のみ)。
Betmigaの外観とパックの内容の説明
Betmiga 25 mg徐放性フィルムコーティング錠は、茶色と楕円形の錠剤で、同じ面に会社のロゴと「325」が刻印されています。 Betmiga 50 mg徐放性フィルムコーティング錠は、黄色と楕円形の錠剤で、同じ面に会社のロゴと「355」が刻印されています。
Betmigaは、10、20、30、50、60、90、100、または200錠を含むアルミアルブリスターと、90錠を含むシリカゲル乾燥剤とチャイルドレジスタンスクロージャーを備えた高密度ポリエチレン(HDPE)ボトルで提供されます。
すべてのパックサイズが販売されているわけではありません。お住まいの国ではボトルをご利用いただけない場合があります。
ソースパッケージリーフレット:AIFA(イタリア医薬品庁)。 2016年1月に公開されたコンテンツ。現在の情報は最新ではない可能性があります。
最新バージョンにアクセスするには、AIFA(イタリア医薬品庁)のWebサイトにアクセスすることをお勧めします。免責事項と有用な情報。
01.0医薬品の名前
BETMIGA 25MG徐放性錠剤
▼追加の監視の対象となる医薬品。これにより、新しい安全情報を迅速に特定できます。医療専門家は、疑わしい副作用を報告するように求められます。副作用を報告する方法については、セクション4.8を参照してください。
02.0定性的および定量的組成
各錠剤には25mgのミラベグロンが含まれています。
添加剤の完全なリストについては、セクション6.1を参照してください。
03.0剤形
徐放錠。
茶色の楕円形のタブレットで、同じ面に会社のロゴと「325」が刻印されています。
04.0臨床情報
04.1治療適応
過活動膀胱(OAB)症候群の成人患者に発生する可能性のある、切迫感、頻尿、および/または切迫性尿失禁の対症療法。
04.2投与の形態と方法
投与量
成人(高齢者を含む)
推奨用量は、食物の有無にかかわらず、1日1回50mgです。
特別な人口
腎臓および肝臓の機能障害
Betmigaは、末期腎疾患(GFR 2または血液透析を必要とする患者)または重度の肝機能障害(Child-PughクラスC)の患者では研究されていないため、これらの患者集団での使用は推奨されません(4.4項および5.2項を参照)。
次の表は、強力なCYP3A阻害剤の存在下または非存在下での肝機能障害または腎機能障害のある患者の1日量の推奨事項を示しています(セクション4.4、4.5、および5.2を参照)。
1.軽度:60〜89 mL / min / 1.73m2の糸球体濾過率(GFR)。中程度:GFR 30〜59 mL /分/1.73m2;重度:GFR 15〜29 mL /分/1.73m2。
2.軽度:チャイルドピュークラスA;中程度:チャイルドピュークラスB。
3.強力なCYP3A阻害剤については、セクション4.5を参照してください。
セックス
性別に基づいて用量を調整する必要はありません。
小児人口
18歳未満の子供におけるミラベグロンの安全性と有効性はまだ確立されていません。
利用可能なデータはありません。
投与方法
錠剤は、液体と一緒に1日1回服用し、丸ごと飲み込んでください。噛んだり、割ったり、壊したりしないでください。
04.3禁忌
活性物質またはセクション6.1に記載されている賦形剤のいずれかに対する過敏症。
04.4使用に関する特別な警告と適切な注意事項
腎機能障害
Betmigaは、末期腎疾患の患者(GFR 2または血液透析を必要とする患者)では研究されていないため、この患者集団での使用は推奨されていません。重度の腎機能障害(GFR 15〜29 mL /分/1.73 m2)の患者のデータは限られています。この集団における薬物動態研究(セクション5.2を参照)に基づいて、25mgへの用量減少が推奨されます。 Betmigaの使用は、強力なCYP3A阻害剤を同時に投与されている重度の腎機能障害(GFR 15〜29 mL / min / 1.73 m2)の患者には推奨されません(セクション4.5を参照)。
肝機能障害
Betmigaは、重度の肝機能障害のある患者(Child-PughクラスC)で研究されていないため、この患者集団での使用は推奨されていません。Betmigaの使用は、中等度の腎機能障害のある患者(Child-PughのクラスB)では推奨されていません。 )強力なCYP3A阻害剤を同時に投与されている人(セクション4.5を参照)。
高血圧
Betmigaは、重度の管理されていない高血圧症(収縮期血圧≥180mmHgおよび/または拡張期血圧≥110mmHg)の患者では評価されていません。したがって、これらの患者への使用は推奨されません。ステージ2の高血圧症(収縮期血圧≥160mmHgおよび/または拡張期血圧≥100mmHg)の患者では、データが限られています。
先天性または後天性のQT間隔延長のある患者
臨床試験では、治療用量でのBetmigaの投与は、臨床的に関連するQT間隔の延長を引き起こしませんでした(セクション5.1を参照)。QT間隔を延長することが知られている薬を服用している患者、したがってこれらの患者におけるミラベグロンの効果は不明です。注意これらの患者にミラベグロンを投与する場合に使用する必要があります。
OABのために抗ムスカリン薬を服用している頸部尿道閉塞の患者
市販後では、膀胱出口部閉塞(BOO)のある被験者とOABを治療するために抗ムスカリン薬を服用している被験者でミラベグロンを服用している患者で尿閉の症例が報告されています。 Betmigaで治療;ただし、臨床的に重大なBOOの患者には、Betmigaの投与には注意が必要です。また、OABの治療のために抗ムスカリン薬を服用している患者には、Betmigaの投与にも注意が必要です。
04.5他の医薬品との相互作用および他の形態の相互作用
データ 試験管内で
ミラベグロンは、複数の経路を介して輸送および代謝されます。ミラベグロンは、チトクロームP450 CYP3A4、CYP2D6、ブチリルコリンエステラーゼ、ウリジン二リン酸グルクロノシルトランスフェラーゼ(UGT)、細胞外膜輸送体P糖タンパク質(P-gp)、細胞内有機カチオン輸送体(OCT)OCT1、OCT2、OCT3の基質です。 。ヒト肝ミクロソームおよび組換えヒトCYPにおけるミラベグロンを用いた研究は、ミラベグロンがCYP2D6の中程度で時間依存性の阻害剤であり、CYP3Aの弱い阻害剤であることを示しています。高濃度では、ミラベグロンはP-gpを介した薬物輸送を阻害しました。
データ インビボ
CYP2D6多型
CYP2D6の遺伝子多型は、ミラベグロンへの平均血漿曝露に最小限の影響しか与えません(セクション5.2を参照)。ミラベグロンと既知のCYP2D6阻害剤との相互作用は予想されておらず、研究されていません。 CYP2D6阻害剤と一緒に投与された場合、またはCYP2D6の代謝が不十分な患者では、ミラベグロンの用量調整は必要ありません。
薬物間の相互作用
ミラベグロンの薬物動態に対する同時投与された薬物の効果、および同時投与された薬物の薬物動態に対するミラベグロンの効果は、単回投与および反復投与の研究で評価された。ほとんどの薬物相互作用は、制御された経口吸収システム(OCAS)錠剤として100mgの用量でミラベグロンを投与することによって研究されてきました。
ミラベグロンとメトプロロールおよびメトホルミンとの相互作用研究では、ミラベグロン即時放出(IR)160mgを使用しました。
ミラベグロンと、CYPアイソザイムまたはトランスポーターの1つの基質を阻害、誘導、または基質とする医薬品との間の臨床的に関連する相互作用は、CYP2D6基質の代謝に対するミラベグロンの阻害効果を除いて期待されていません。
酵素阻害剤の効果
ミラベグロン曝露(AUC)は、健康なボランティアにおいて強力なCYP3A / P-gpケトコナゾール阻害剤の存在下で1.8倍に増加しました。ベトミガをCYP3Aおよび/またはP-gp阻害剤と組み合わせて投与する場合、用量調整は必要ありません。 D "一方、軽度から中等度の腎機能障害(GFR 30〜89 mL / min / 1.73 m2)または中等度の肝機能障害(Child-Pough Class A)の患者で、イトラコナゾール、ケトコナゾール、リトナビルなどのCYP3Aの強力な阻害剤を同時に投与されているクラリスロマイシンの場合、推奨される1日量は25 mgで、食事の有無にかかわらず1日1回です(セクション4.2を参照)。 Betmigaは、重度の腎機能障害(GFR 15〜29 mL / min / 1.73 m2)の患者、またはCYP3A阻害剤を同時に投与されている中等度の肝機能障害(Child-Pough Class B)の患者には推奨されません(セクション4.2および4.4を参照)。
酵素誘導剤の効果
CYP3AまたはP-gpの誘導物質である物質は、ミラベグロンの血漿濃度を低下させます。ミラベグロンがリファンピシンまたは他のCYP3AまたはP-gpの誘導物質とともに治療用量で投与される場合、用量調整は必要ありません。
CYP2D6基質に対するミラベグロンの効果
健康なボランティアでは、CYP2D6に対するミラベグロンの阻害効力は中程度であり、CYP2D6活性は、ミラベグロンの中止後15日以内に回復します。ミラベグロンIRの日用量を繰り返し投与すると、Cmaxが90%増加し、AUCの229%が増加します。メトプロロールの単回投与。ミラベグロンの1日量を繰り返し投与すると、デシプラミンの単回投与でCmaxが79%増加し、AUCが241%増加します。
ミラベグロンが治療指数の狭い医薬品と同時投与され、チオリダジン、C1型抗不整脈薬(フレカイニド、プロパフェノンなど)、三環系抗うつ薬(イミプラミン、デシプラミンなど)などのCYP2D6によって有意に代謝される場合は注意が必要です。ミラベグロンをCYP2D6基質と同時投与する場合も注意が必要です。CYP2D6基質の用量は個別に滴定されます。
トランスポーターに対するミラベグロンの効果
ミラベグロンは弱いP-gp阻害剤です。健康なボランティアでは、ミラベグロンはCmaxとAUCをP-gp基質ジゴキシンの29%と27%増加させます。ベトミガとジゴキシンの組み合わせを服用し始めた患者では、最初に低用量のジゴキシンを処方する必要があります。
血清ジゴキシン濃度を監視し、ジゴキシンの用量漸増に使用して、望ましい臨床効果を達成する必要があります。ベトミガをP-gpに感受性のあるサブスタートと組み合わせた場合の、P-gpに対するミラベグロンの阻害能を考慮する必要があります。 。
その他の相互作用
ミラベグロンを治療用量のソリフェナシン、タムスロシン、ワルファリン、メトホルミン、またはエチニルエストラジオールとレボノルゲストレルを含む経口避妊薬の組み合わせと同時投与した場合、臨床的に関連する相互作用は観察されませんでした。用量調整はお勧めしません。
薬物間相互作用によって引き起こされるミラベグロンへの曝露の増加は、脈拍数の増加と関連している可能性があります。
04.6妊娠と授乳
妊娠
妊娠中の女性におけるベトミガの使用に関するデータは限られています。動物実験では生殖毒性が示されています(セクション5.3を参照)。妊娠中および避妊手段を使用していない出産の可能性のある女性にはベトミガは推奨されません。
えさの時間
ミラベグロンはげっ歯類の乳汁中に排泄されるため、母乳中に存在すると予想されます(セクション5.3を参照)。ミラベグロンがヒトの母乳生産に与える影響、母乳中の存在、または母乳で育てられた乳児への影響を調査するための研究は行われていません。授乳中はベトミガを投与しないでください。
受胎能力
動物では、ミラベグロン治療に関連した出産への影響は観察されませんでした(セクション5.3を参照)。ミラベグロンが人間の出産に及ぼす影響は確立されていません。
04.7機械の運転および使用能力への影響
Betmigaは、機械を運転または使用する能力にまったくまたは無視できる影響を及ぼします。
04.8望ましくない影響
安全性プロファイルの要約
Betmigaの安全性はOABの8,433人の患者で評価されました。そのうち5,648人は臨床プログラムのフェーズ2/3の間に少なくとも1回のミラベグロンの投与を受け、622人の患者は少なくとも1年間(365日)Betmigaを受けました。 3つの第3相二重盲検プラセボ対照12週間試験では、88%の患者がBetmigaによる治療を完了し、4%が有害事象のために治療を中止しました。ほとんどの反応は軽度から中等度の実体でした。
3つの第3相二重盲検プラセボ対照12週間試験中にベトミガ50mgで治療された患者で報告された最も一般的な副作用は、頻脈と尿路感染症でした。頻脈の頻度は、ベトミガ50mgを投与された患者で1.2%でした。頻脈は、ベトミガ50mgを投与された患者の0.1%で治療中止を引き起こしました。ベトミガ50mgを投与された患者の尿路感染症の頻度は2.9%でした。尿路感染症は、ベトミガ50mgを投与された患者のいずれにおいても治療中止を引き起こしませんでした。重篤な副作用には心房細動(0.2%)が含まれていました。
1年間(長期)の活性物質(ムスカリン拮抗薬)試験中に観察された有害反応は、3つの12週間の二重盲検プラセボ対照第3相試験で観察されたものとタイプおよび重症度が類似していた。
副作用の表
以下の表は、3つの12週間の二重盲検プラセボ対照第3相試験で観察された副作用を示しています。
副作用の頻度は次のように定義されています。非常に一般的(≥1/ 10)。一般的(≥1/ 100、
同じ頻度グループ内で、副作用は重症度の降順でリストされています。
*市販後の経験で観察された
疑わしい副作用の報告
医薬品の承認後に発生した疑わしい副作用の報告は、医薬品のベネフィット/リスクバランスを継続的に監視できるため重要です。医療専門家は、国の報告システムを介して疑わしい副作用を報告するよう求められます。
04.9過剰摂取
ミラベグロンは、400mgまでの単回投与で健康なボランティアに投与されています。この用量で記録された有害事象には、動悸(1/6被験者)および100拍/分(bpm)を超える脈拍の増加(3/6被験者)が含まれていました。健康なボランティアに投与した場合、1日あたり最大300 mgのミラベグロンを10日間複数回投与すると、脈拍と収縮期血圧の上昇が見られました。
過剰摂取の治療は、対症療法と支持療法でなければなりません。過剰摂取の場合は、脈拍、血圧、心電図を監視することをお勧めします。
05.0薬理学的特性
05.1薬力学的特性
薬物療法グループ:泌尿器科、尿鎮痙薬。 ATCコード:G04BD12。
作用機序
ミラベグロンは、ベータ3アドレナリン受容体の強力かつ選択的なアゴニストです。ミラベグロンは、単離されたラットおよびヒト組織の膀胱平滑筋の弛緩、ラット膀胱組織の環状アデノシン一リン酸(cAMP)の濃度の増加をもたらし、膀胱に弛緩効果を示しました。ラット膀胱モデルにおいて。
ミラベグロンは、ラット過活動膀胱モデルの排尿圧や残尿に影響を与えることなく、排尿あたりの平均排尿量を増やし、排尿を引き起こさない収縮の頻度を減らしました。サルモデルでは、ミラベグロンは排尿頻度の低下を示しました。これらの結果は、ミラベグロンが改善することを示しています。膀胱内のベータ3アドレナリン作動性受容体を刺激することによる尿貯蔵機能。
蓄積段階、つまり膀胱に尿が蓄積すると、交感神経の刺激が一般的になります。ノルアドレナリンは神経終末から放出され、膀胱筋のベータアドレナリン受容体の活性化を主に決定します。膀胱の平滑筋。空になる段階では、膀胱は主に副交感神経系によって制御されます。骨盤神経終末から放出されるアセチルコリンは、コリン作動性受容体M²およびM³を刺激し、膀胱の収縮を誘発します。M²の活性化。また、ベータ3アドレナリン受容体によって誘発されるcAMPの増加を阻害します。したがって、ミラベグロンが収縮の頻度を減少させた部分的な尿道閉塞のラットで確認されたように、ベータ3アドレナリン受容体の刺激は排出プロセスを妨げないはずです。排尿あたりの排尿量、排尿圧または残留尿量に影響を与えることなく。
薬力学的効果
尿流動態
下部尿路症状(LUTS)および頸部尿道閉塞(BOO)の男性被験者に50mgおよび100mgの用量で1日1回12週間投与されたベトミガは、膀胱内圧測定パラメーターに影響を示さず、安全で忍容性が良好でした。最大流量および最大流量での排尿筋圧に対するミラベグロンの効果は、LUTSおよびBOOの男性患者200人を対象とした尿流動態検査で評価されました。ミラベグロンを50mgおよび100mgの用量で1日1回12週間投与しても、最大流量または最大流量での排尿筋圧に悪影響はありませんでした。 LUTS / BOOの男性患者を対象としたこの研究では、ベースラインから排尿後の残存量(mL)の治療終了までの調整平均変化(SE)は、プラセボ群で0.55、17.89、30.77でした。ミラベグロン50mgおよびミラベグロン100 mg。
QT間隔への影響
50mgおよび100mgの用量のBetmigaは、性別またはグループ全体で評価された心拍数の個別に修正されたQT間隔(QTcI間隔)に影響を与えませんでした。
徹底的なQT(TQT)研究(n = 164人の健康な男性ボランティアとn = 153人の平均年齢33歳の健康な女性ボランティア)は、示された用量でのミラベグロンの反復経口投与(1日1回50 mg)の効果を評価しました。 QTcI間隔での2つの超治療用量(1日1回100mgおよび200mg)。超治療用量は、治療用量曝露のそれぞれ約2.6倍および6.5倍です。モキシフロキサシンの単回400mg用量を陽性対照として使用した。ミラベグロンとモキシフロキサシンの各用量レベルは、両方ともプラセボ対照(並行クロスオーバーデザイン)を用いて、別々の治療群で評価されました。 50mgおよび100mgの用量でミラベグロンを投与された男性および女性の被験者の場合、95%信頼区間の上限である片側試験は、関連する最大平均差についていつでも10ミリ秒を超えませんでした。時間対プラセボQTcI間隔で。ミラベグロンを50mgの用量で投与された女性被験者では、投与後5時間のQTcI間隔におけるプラセボとの平均差は3.67ミリ秒でした(95%信頼区間片側試験の上限、5.72ミリ秒)。男性被験者では、差は2.89ミリ秒でした(95%信頼区間の上限、片側検定、4.90ミリ秒)。200mgのミラベグロンの用量では、QTcI間隔は男性被験者ではいつでも10ミリ秒を超えませんでした。一方、女性の被験者では、片側95%信頼区間の上限が0.5〜6時間で10ミリ秒を超え、平均効果が10.42ミリ秒であった5時間のプラセボとの最大差がありました(95%信頼区間の上限)間隔、片側検定、13.44ミリ秒)。QTcFおよびQTcIfの結果は、QTcI間隔と一致していました。
このTQT研究では、ミラベグロンは、50mgから200mgの試験用量範囲でECGの心拍数の用量依存的な増加をもたらしました。心拍数のプラセボに対する最大平均差は、ミラベグロン50mgで17.3で6.7bpmの範囲でした。健康な被験者におけるミラベグロン200mgのbpm。
OAB患者の脈拍と血圧への影響
Betmiga 50 mgを1日1回投与されたOAB患者(平均年齢:59歳)を対象とした3つの第3相二重盲検プラセボ対照12週間試験では、平均差の増加が観察されました。パルスの場合は1bpm、収縮期血圧/拡張期血圧(SBP / DBP)の場合は約1mmHg以下。脈拍と血圧の変化は、治療を中止すると元に戻せます。
眼圧(IOP)への影響
1日1回投与されたミラベグロン100mgは、56日間の治療後に健康な被験者のIOPの増加を示さなかった。 310人の健康な被験者におけるゴールドマン圧平眼圧測定によるIOPに対するベトミガの効果を評価する第1相試験では、ベースラインから平均56日目までの平均変化における治療差の主要評価項目について、100mg用量のミラベグロンはプラセボより劣っていませんでした。 /サブジェクトIOP; 95%信頼区間の上限、ミラベグロン100mgとプラセボの治療差の両側試験は0.3mmHgでした。
臨床効果と安全性
Betmigaの有効性は、失禁の有無にかかわらず、切迫感と頻度の症状に関連する過活動膀胱症候群の治療に関する3つのランダム化二重盲検プラセボ対照12週間第3相試験で評価されました。平均年齢59歳(年齢範囲:18-95歳)の女性(72%)および男性(28%)の患者が含まれました。研究対象集団は、以前に抗ムスカリン療法を受けたことがない患者の約48%および約52%で構成されていました。以前に抗ムスカリン薬で治療された患者による1つの研究では、495人の患者が活性対照薬(トルテロジン徐放製剤)を投与されました。
主要な有効性エンドポイントは、以下から構成されていました。治療終了時の24時間の失禁エピソードの平均数のベースラインからの変化。 3日間の完了した排尿日誌に基づく24時間あたりの平均排尿回数のベースラインから治療終了までの変化ミラベグロンは、共同一次エンドポイントと二次エンドポイントの両方でプラセボと比較して統計的に有意な改善を示しました(表1および2を参照) 。
表1:統一された研究のために治療の最後に選択された共同一次および二次有効性エンドポイント
統一された研究は、046(EU /オーストラリア)、047(北アメリカ[NA])、074(EU / NA)の研究で構成されていました。
†最小二乗法は、ベースライン、性別、および研究に合わせて調整されたことを意味します。
*多重度補正なしの0.05レベルで、プラセボよりも統計的に有意に高い。
#0.05の多重度補正レベルでプラセボより統計的に有意に高い。
FAS:完全分析セット、二重盲検で少なくとも1用量の治験薬を投与され、ベースライン日誌に排尿測定値があり、ベースライン後の訪問日誌に少なくとも1回排尿測定値があるランダム化されたすべての患者。
FAS-I:ベースラインの日記に少なくとも1回の失禁エピソードがあるFASのサブグループ。
CI:信頼区間
表2:試験046、047および074の治療終了時に選択された共同一次および二次有効性エンドポイント
†最小二乗法は、ベースライン、性別、および地理的地域に合わせて調整されていることを意味します。
*多重度補正なしの0.05レベルでプラセボよりも統計的に有意に高い。
#0.05の多重度補正レベルでプラセボより統計的に有意に高い。
‡統計的観点から、0.05の多重度補正レベルでのプラセボに対する有意でない優位性。
FAS:完全な分析セット、ベースラインで二重盲検および排尿日記で少なくとも1用量の治験薬を投与され、排尿計算を伴うベースライン後の訪問日記で少なくとも1回投与されたすべてのランダム化患者。
FAS-I:ベースラインの日記に少なくとも1回の失禁エピソードがあるFASのサブグループ。
Betmiga 50 mgを1日1回投与すると、4週目の最初の検出で有効であり、12週間の治療期間を通じて有効性が維持されました。長期のランダム化比較試験では、1年間の治療期間を通じて有効性が維持されていることが示されました。
健康に関連した生活の質のパラメーターの主観的改善
3つのフェーズ3、二重盲検、プラセボ対照、12週間の研究では、ミラベグロンを1日1回投与したOAB症状の治療により、以下の健康関連の生活の質のパラメーターにおいて、プラセボと比較して統計的に有意な改善が見られました。症状の治療と不快感。
OABの治療のために抗ムスカリン療法を受けたことがある、または受けたことがない患者における有効性
ミラベグロンは、OABの治療のために抗ムスカリン療法を受けている患者と受けていない患者の両方で有効性が実証されています。ミラベグロンは、効果が不十分なためにOABの治療のために抗ムスカリン療法による治療を以前に中止した患者でも有効であることが示されています(表を参照) 3)。
表3:OABの治療のために以前に抗ムスカリン療法を受けていた患者の主要な有効性エンドポイント
統一された研究は、046(EU /オーストラリア)、047(北アメリカ[NA])、074(EU / NA)の研究で構成されていました。
†最小二乗平均は、プールされた研究のベースライン、性別、研究、サブグループ、治療相互作用サブグループに対して調整され、最小二乗平均は、研究046のベースライン、性別および地理的領域、サブグループ、治療相互作用サブグループに対して修正された平均です。
FAS:完全な分析セット、ベースラインで二重盲検および排尿日記で少なくとも1用量の治験薬を投与され、排尿測定を伴うベースライン後の訪問日記で少なくとも1回投与されたすべてのランダム化患者。
FAS-I:ベースラインの日記に少なくとも1回の失禁エピソードがあるFASのサブグループ。
小児人口
欧州医薬品庁は、「特発性過活動膀胱症候群の治療」および「神経性排尿筋過活動の治療」の適応症において、小児集団の1つまたは複数のサブセットにおけるベトミガの研究結果を提出する義務を延期しました(セクション4.2を参照)小児の使用に関する情報)。
05.2薬物動態特性
吸収
健康なボランティアに経口投与した後、ミラベグロンは吸収され、3〜4時間でピーク血漿濃度(Cmax)に達します。絶対バイオアベイラビリティは、25 mgの用量での29%から50 mgの用量での35%に増加しました。平均CmaxとAUCは、用量範囲全体で用量よりも比例して増加しました。男性と女性の合計人口では、ミラベグロンの用量が50mgから100mgに2倍に増加すると、CmaxとAUCtauが約2.9増加しました。ミラベグロンの投与量を50mgから200mgに4倍に増やすと、それぞれ2.6倍と2.6倍になり、CmaxとAUCtauが約8.4倍と6.5倍に増加しました。での濃度 定常状態 ミラベグロンの1日1回投与から7日以内に達成されます。 1日1回の投与後、定常状態でのミラベグロンの血漿曝露は、単回投与後に観察されたものの約2倍です。
吸収に対する食物の影響
50mgの錠剤と高脂肪の食事を併用すると、ミラベグロンのCmaxとAUCがそれぞれ45%と17%減少しました。低脂肪の食事では、ミラベグロンのCmaxとAUCが75%減少しました。それぞれ51%。第3相試験では、ミラベグロンは食物の有無にかかわらず投与され、安全で効果的であることが証明されました。したがって、ミラベグロンは、推奨用量で食物の有無にかかわらず摂取することができます。
分布
ミラベグロンは広く分布しています。での分布容積 定常状態 (Vss)は約1670 Lです。ミラベグロンはヒト血漿タンパク質に結合し(約71%)、アルブミンおよびα-1酸性糖タンパク質に対して中程度の親和性を示します。ミラベグロンは赤血球に分布しています。赤血球 試験管内で 14C-ミラベグロンの割合は血漿中の約2倍でした。
生体内変化
ミラベグロンは、脱アルキル化、酸化、(直接)グルクロン酸抱合、およびアミド加水分解を含む複数の経路を介して代謝されます。ミラベグロンは、14C-ミラベグロンの単回投与後の主要な循環成分です。 2つの主要な代謝物がヒト血漿で観察されています。どちらもフェーズ2グルクロニドであり、それぞれ総曝露量の16%と11%を占めています。これらの代謝物は薬理学的に活性ではありません。
研究に基づく 試験管内で、ミラベグロンは臨床的に検出できない濃度でこれらの酵素の活性を阻害しないため、ミラベグロンはシトクロムP450酵素によって同時投与される医薬品の代謝を阻害しないようです:CYP1A2、CYP2B6、CYP2C8、CYP2C9、CYP2C19およびCYP2E1。 OCTを介した薬物トランスポーターの臨床的に有意な阻害を引き起こすとは予想されていません。
研究が 試験管内で ミラベグロンの酸化的代謝におけるCYP2D6とCYP3A4の役割を示唆している、結果 インビボ これらのアイソザイムが全体的な除去において限定的な役割を果たしていることを示しています。 試験管内で と exvivo CYP3A4とCYP2D6に加えて、ミラベグロンの代謝におけるブチリルコリンエステラーゼ、UGT、そしておそらくアルコールデヒドロゲナーゼ(ADH)の関与を示しました。
CYP2D6多型
CYP2D6基質の代謝が遺伝的に乏しい健康な被験者(CYP2D6の阻害の代わりに使用)では、ミラベグロンIR製剤の160 mgの単回投与の平均CmaxおよびAUCinfは、強力な代謝物質よりも14%および19%高かった。 CYP2D6遺伝子多型は、ミラベグロンへの平均血漿曝露に最小限の影響しか及ぼさないことを示しています。ミラベグロンと既知のCYP2D6阻害剤との相互作用は予測できず、研究されていません。 CYP2D6阻害剤と一緒に投与された場合、またはCYP2D6の代謝が不十分な患者では、ミラベグロンの用量調整は必要ありません。
排除
血漿の全身クリアランス(CLtot)は約57 L / hです。最終排泄半減期(t1 / 2)は約50時間です。腎クリアランス(CLR)は約13 L / hで、CLtotの約25%に相当します。ミラベグロンの腎排泄は、主に糸球体濾過を伴う活発な尿細管分泌によって起こります。未変化のミラベグロンの尿中排泄は用量依存的であり、25mgの1日投与後の約6.0%から100mgの1日投与後の12.2%の範囲です。健康なボランティアに160mgの14C-ミラベグロンを投与した後、放射性標識剤は尿中に回収され、34%が糞便中に回収されました。変化のないミラベグロンは尿中放射能の約45%を占め、代謝物の存在を示しています。変更されていないミラベグロンが糞便中の放射能の大部分を占めていました。
年
高齢のボランティア(65歳以上)に複数回経口投与した後のミラベグロンとその代謝物のCmaxとAUCは、若いボランティア(18〜45歳)のものと同様でした。
セックス
CmaxとAUCは、男性よりも女性の方がそれぞれ約40〜50%高くなっています。性別によるCmaxとAUCの違いは、体重と生物学的利用能の違いに起因します。
人種
ミラベグロンの薬物動態は人種の影響を受けません。
腎機能障害
軽度の腎機能障害のあるボランティアに100mgのベトミガを単回投与した後(腎疾患における食事療法の変更(MDRD)研究で推定されたeGFR 60〜89 mL / min / 1.73 m2)、ミラベグロンの平均CmaxおよびAUCそれは
腎機能が正常なボランティアと比較して、それぞれ6%と31%増加しました。中等度の腎機能障害(eGFR-MDRD 30〜59 mL / min / 1.73 m2)のボランティアでは、CmaxとAUCがそれぞれ23%と66%増加しました。重度の腎機能障害のあるボランティア(eGFR-MDRD 15〜29 mL / min)では/ 1.73 m2)、平均CmaxとAUCはそれぞれ92%と118%高かった。ミラベグロンは、末期腎疾患の患者(GFR 2または血液透析を必要とする患者)では研究されていません。
肝機能障害
軽度の肝機能障害のあるボランティア(チャイルドピュークラスA)に100 mgのベトミガを単回投与した後、ミラベグロンの平均CmaxとAUCは、正常な肝機能を持つボランティアと比較して、それぞれ9%と19%増加しました。中等度の肝機能障害(チャイルドピュークラスB)では、平均CmaxとAUCはそれぞれ175%と65%高かった。ミラベグロンは、重度の肝機能障害(チャイルドピュークラスC)の患者では研究されていません。
05.3前臨床安全性データ
前臨床試験では、臨床観察と互換性のある毒性標的臓器が特定されています。ラットでは、肝臓酵素の一時的な増加と肝細胞の変化(壊死とグリコーゲン粒子の減少)が観察されました。心拍数の増加は、ラットだけでなく、ウサギ、イヌ、サルでも観察されました。遺伝子毒性および発がん性の研究では、遺伝子毒性または発がん性の可能性は明らかにされませんでした インビボ.
致死量以下の用量(最大推奨ヒト等価線量の19倍、最大ヒト推奨用量MHRD)では、MHRDで観察されたものの36倍の全身曝露で出産性の障害は観察されなかった。心臓肥大)さらに、肺奇形(付属品の欠如)ウサギでは、MHRDの14倍の全身暴露で移植損失の増加が観察されたが、骨化に対する可逆的影響(波状肋骨、骨化の遅延、胸骨、中手骨または中足骨の骨化部分の数の減少)が認められた。 MHRDより22倍高い全身暴露でのラット。胚-胎児毒性は、母体毒性に関連する用量で検出された。ウサギで観察された心血管奇形は、ベータ1アドレナリン受容体の活性化によって媒介されることが示されています。
放射性標識ミラベグロンを用いた薬物動態研究では、親化合物および/またはその代謝物が、投与後4時間の血漿レベルの約1.7倍のレベルでラット乳汁中に排泄されることが示されています(セクション4.6を参照)。
06.0医薬品情報
06.1添加剤
タブレットのコア
Macrogol
ヒドロキシプロピルセルロース
ブチルヒドロキシトルエン
ステアリン酸マグネシウム
コーティング
ヒプロメロース
Macrogol
黄色の酸化鉄(E172)
赤い酸化鉄(E172)
06.2非互換性
関係ありません。
06.3有効期間
3年
最初にボトルを開けてからの貯蔵寿命:6ヶ月
06.4保管に関する特別な注意事項
この薬は特別な保管条件を必要としません。
06.5即時包装の性質および包装の内容
10、20、30、50、60、90、100、または200錠を含むカートン内のアルミアルブリスター。
チャイルドレジスタンスポリプロピレン(PP)キャップと90錠を含むシリカゲル乾燥剤を備えたHDPEボトル。
すべてのパックサイズが販売されているわけではありません。
06.6使用および取り扱いに関する指示
未使用の薬やこの薬に由来する廃棄物は、地域の規制に従って処分する必要があります。
07.0マーケティング承認保持者
アステラス製薬ヨーロッパB.V.
Sylviusweg 62
2333BEライデン
オランダ
08.0マーケティング承認番号
EU / 1/12/809 / 001-007
042647014
042647026
042647038
042647040
042647053
042647065
042647077
EU / 1/12/809/015
042647154
EU / 1/12/809/016
042647166
09.0最初の承認または承認の更新の日付
最初の承認日:2012年12月20日
10.0本文の改訂日
D.CCE 2014年11月