Jetreaとは何ですか?また、それは何に使用されますか?
Jetreaは、有効成分のオクリプラスミンを含む薬です。成人では、重度の視覚障害を引き起こす可能性のある眼疾患である硝子体牽引(VMT)の治療に適応されます。
Jetreaはどのように使用されますか-Ocriplasmina?
Jetreaは、眼球注射用の溶液に作られる濃縮物です。薬は処方箋でのみ入手でき、硝子体内注射(硝子体への注射、目の後ろのゼラチン状の塊)の経験を持つ眼科医(眼疾患の専門家)が準備して投与する必要があります。濃縮物は冷凍庫に保管する必要があり、手順は無菌条件下で行う必要があります。
推奨用量は、影響を受けた眼に単回投与として1回だけ注射して0.125 mgを投与することです。もう一方の眼は、少なくとも7日間はJetreaで治療しないでください。
眼科医は、眼の感染を防ぐために、ジェットレアによる治療の前後に抗生物質の点眼薬を処方する場合があります。感染や眼内圧の上昇を除外するために、注射後に患者を監視する必要があります。
Jetrea-Ocriplasminaはどのように機能しますか?
硝子体牽引は硝子体接着(VMA)によって引き起こされ、硝子体は網膜の中心部(眼の最も内側の膜、光に敏感)に異常な力で付着したままになります。体の硝子体収縮のサイズそして、異常な付着によって影響を受けた領域は、網膜に牽引力を及ぼす可能性があり、それは次に、網膜自体の腫れ、および視力のぼやけまたは歪みなどの症状を引き起こす。
Jetreaの有効成分であるオクリプラスミンは、硝子体と網膜の間の接着に関与するタンパク質を分解し、それによって腫れを減らし、視力を改善することができる、眼に自然に存在する酵素であるヒトプラスミンに似ています。
Jetreaのオクリプラスミンは、「組換えDNA技術」として知られる方法で生産されます。これは、オクリプラスミンの生産を可能にする遺伝子(DNA)を受け取った酵母細胞によって作られます。
Jetrea-Ocriplasminは研究中にどのような利点を示しましたか?
研究中、Jetreaは硝子体と網膜の間の癒着を効果的に解消し、手術の必要性を減らすことが示されました。
VMAと視力低下のある成人652人を対象とした2つの主要な研究では、硝子体内注射により、患者にJetreaまたはプラセボ(ダミー治療)を0.125mg単回投与しました。
28日後、プラセボで治療された被験者の13%と6%(107人中14人)と比較して、Jetreaの注射で治療された患者の25%と28%(219人中61人と245人中62人)で癒着が治癒しました。および81の5)VMAの効果的な治療は、VMTによって引き起こされる視力障害を解決し、進行性の未治療の網膜牽引に関連するさらなる視力喪失を防ぐのに役立ちます。
Jetrea-Ocriplasminaに関連するリスクは何ですか?
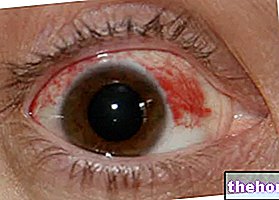
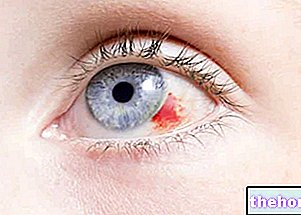
Jetreaで見られる副作用は目に影響を与えます。Jetreaの最も一般的な副作用は、飛んでいるハエ(視野内の暗くて不規則な形のスポット)、目の痛み、光視症(視野内の閃光の形での光感覚)です。 )および結膜下出血(眼球を覆う膜からの出血)。Jetreaで報告された副作用の完全なリストについては、パッケージのリーフレットを参照してください。
Jetreaは、眼の中または周囲に感染が知られている、または疑われる患者には使用しないでください。制限の完全なリストについては、添付文書を参照してください。
Jetrea-Ocriplasminaが承認されたのはなぜですか?
エージェンシーのヒト用医薬品委員会(CHMP)は、Jetreaの利点はリスクよりも大きいと結論付け、EUでの使用を承認することを推奨しました。研究によると、Jetreaは硝子体癒着の治療に有効であり、したがって医薬品製品は、未治療の進行性硝子体牽引の存在下で発生する可能性のある視覚障害のエピソードを予防するのに効果的であると期待されています。控えめですが(患者の4分の1でVMAの解消)、Jetreaによる治療は視力を改善し、手術を回避できるため、この薬の利点は重要であると考えられました。薬の安全性に関しては、短命で管理可能と考えられている最も一般的な副作用は、注射手順に続発するか、病気自体の解決に関連していることがよくあります。視力の不可逆的な低下、網膜の機能またはレンズの支持構造における他の変化などのより深刻な副作用のリスクは減少しているように見えます。
Jetrea-Ocriplasminの安全で効果的な使用を確実にするためにどのような対策が取られていますか?
Jetreaが可能な限り安全に使用されることを保証するために、リスク管理計画が作成されました。この計画に基づいて、医療専門家と患者が従うべき適切な注意事項を含む、安全性情報がJetreaの製品特性と添付文書の要約に追加されました。
さらに、Jetreaを製造する会社は、Jetreaを使用する可能性のあるすべての医療専門家が、薬の使用方法に関する基本情報を含む情報パックと、患者に渡すための情報パックを確実に受け取る必要があります。
Jetreaに関するその他の情報-Ocriplasmina
2013年3月13日、欧州委員会は、欧州連合全体で有効なJetreaの「販売承認」を発行しました。
Jetrea療法の詳細については、添付文書(EPARに含まれています)を読むか、医師または薬剤師に連絡してください。
この要約の最終更新日:2013年3月。
このページで公開されているJetrea-Ocriplasminaに関する情報は、古くなっているか、不完全である可能性があります。この情報の正しい使用法については、免責事項と有用な情報のページを参照してください。







-funzione-e-uso-clinico.jpg)