ジョバンニ・チェッタ博士が編集
ECMは一般に、いくつかの大きなクラスの生体分子で構成されていると説明されています。
- 構造タンパク質(コラーゲンとエラスチン)
- 特殊なタンパク質(フィブリリン、フィブロネクチン、ラミニンなど)
- プロテオグリカン(アグリカン、シンデカン)およびグルサミノグリカン(ヒアルロン酸、コンドロイチン硫酸、ヘパラン硫酸など)
構造タンパク質
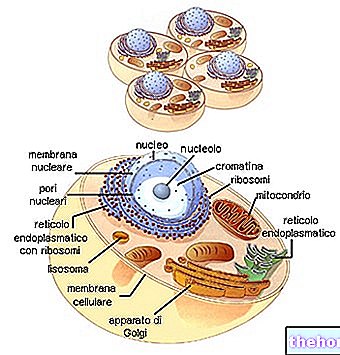
コラーゲンは、動物界で最も代表的な糖タンパク質のファミリーを形成します。それらは細胞外マトリックスに最も存在するタンパク質であり(しかし最も重要ではありません)、適切な結合組織(軟骨、骨、筋膜、腱、靭帯)の基本的な構成要素です。
コラーゲンには少なくとも16種類あり、そのうちタイプI、II、IIIが典型的なフィブリルのレベルで最も多く存在します(タイプIVは、基底膜の主成分を表す一種の網状組織を形成します)。
コラーゲンは主に線維芽細胞によって合成されますが、上皮細胞もそれらを合成することができます。
コラーゲン繊維は、細胞外マトリックスの他の膨大な量の分子と継続的に相互作用し、細胞の生命の基本となる生物学的連続体を構成します。原線維内の関連するコラーゲンは、張力に抵抗できる構造の形成と維持において主要な役割を果たします。ほぼ非弾性である(グルコサミングリカンは圧縮に対する耐性の作用を実行します)。「筋膜」、人間の姿勢に大きな影響を与えます。コラーゲンが環境の影響に応じて変化する能力のさらなる実証として、例えば、剛性、弾性、抵抗の程度はさまざまですが、FACIT(三重らせんが中断されたフィブリル関連コラーゲン)という用語で定義され、プロテオグリカン(「グルコサミノグリカンとプロテオグリカン」の段落で説明)のように機能するコラーゲンがあります。
コラーゲン繊維は、PG / GAG(プロテオグリカン/グルコサミノグリカン)のコーティングのおかげで、バイオセンサーとバイオコンダクターの特性を備えています。相対的な電荷により、水を結合してイオンを交換する能力が高まり、したがって電気容量が大きくなります。
構造変形を発生させることができる機械的な力は、分子間結合に応力を加え、わずかな電束を生成することを私たちは知っています。 圧電電流 (Athenstaedt、1969年)。このような場合、コラーゲン繊維は凸面に正電荷を、凹面に負電荷を分配し、半導体に変化します(一方向の表面に電子が流れるようにします)。圧電エネルギー(および熱応力によって生成される焦電エネルギー)は、循環イオンによって非常に短い時間(約10-7〜10-9秒)で中和されるため、信号上のPG / GAGの配置電気インパルスの「リピーター」として機能するなど、フィブリルの信号の表面の伝播に決定的です。特に、約の縦方向の周期性。 64 nm(光学顕微鏡ではストリークとして表示されます)により、約64 m / s(高速神経線維の伝導速度に対応)に等しいインパルスの伝播速度が可能になります-Rengling、2001年。コラーゲン原線維の強い双極モーメントそして、それらの共鳴能力(すべてのペプチド構造に共通の特性)、およびMECの低誘電率は、電磁信号の伝達を容易にします。したがって、三次元で遍在するコラーゲンネットワークは、生体電気信号を伝導するという独特の特性も備えています。求心性方向(ECMから細胞へ)またはその逆の、コラーゲン原線維と細胞の間の相対的な配置に基づく空間の3つの次元。
これはすべてリアルタイムのMEC細胞通信システムを表しており、そのような電磁生体信号は重要な生化学的変化を引き起こす可能性があります。たとえば、骨では破骨細胞は圧電的に帯電した骨を「消化」できません(Oschman、2000)。
最後に、細胞は、当然のことながら、継続的かつかなりのエネルギー消費(約70%)で材料を生成し、これは必然的に排出されなければならないことを強調する必要があります。小胞(Albergati、2004)。
脊椎動物の組織の大部分は、強度と弾力性という2つの重要な特性が同時に存在する必要があります。これらの組織のECM内にある弾性繊維の実際のネットワークは、強い牽引力の後に初期状態に戻ることを可能にします。弾性繊維は、臓器またはその一部の伸展性を少なくとも5倍に高めることができます。長くて弾力性のないコラーゲン繊維が弾力性のある繊維の間に散在しており、「組織の牽引による過度の変形」を制限するという正確なタスクがあります。Lエラスチン 弾性繊維の主成分を表します。コラーゲンはプロリンとグリシンが豊富であるため、長さが約750アミノ酸の非常に疎水性のタンパク質ですが、コラーゲンとは異なり、糖化されず、ヒドロキシプロリン残基を多く含み、ヒドロキシリシンは含まれていません。エラスチンは、すべての結合組織のECMに浸透する繊維とラメラで構成される、不規則な3次元形状の実際の生化学的ネットワークとして表示されます。エラスチンは、弾性特性を持つ血管に特に豊富に見られます(ECMのタンパク質です。動脈に存在し、大動脈の総乾燥重量の50%以上を占めます)、靭帯、肺、皮膚に存在します。真皮では、コラーゲンで起こることとは反対に、エラスチンの密度と体積は時間とともに増加する傾向がありますが、古いエラスチンは一般に腫れ、ほとんど腫れ、しばしば断片化された外観と成分の減少を伴って見えます。 (Pasquali Rochetti et al、2004)。平滑筋細胞と線維芽細胞は、細胞外空間に分泌されるその前駆体であるトロポエラスチンの主要な産生細胞です。
「コラーゲンとエラスチン、細胞外マトリックスのコラーゲン繊維」に関する他の記事
- 細胞外マトリックス
- フィブロネクチン、グルコサミノグリカンおよびプロテオグリカン
- 細胞平衡における細胞外マトリックスの重要性
- 細胞外マトリックスと病状の変化
- 結合組織と細胞外マトリックス
- 深筋膜-結合組織
- 筋膜機械受容器および筋線維芽細胞
- 深部筋膜の生体力学
- 姿勢とダイナミックバランス
- テンセグリティとらせん運動
- 下肢と体の動き
- 骨盤位サポートと顎口腔装置
- 臨床例、姿勢の変化
- 臨床例、姿勢
- 姿勢評価-臨床例
- 参考文献-細胞外マトリックスから姿勢まで。結合システムは私たちの真のデウスエクスマキナですか?

















.jpg)

