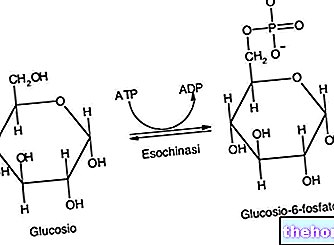
脂肪酸の合成はアセチル補酵素Aから始まり、それらの分解の逆の経路にほぼ対応します。脂肪酸の合成では、一連の重炭酸塩フラグメントが開始アセチル補酵素Aに追加されます。
脂肪酸の合成は完全に細胞質です(つまり、この合成を触媒する酵素は細胞質にあります)。脂肪酸合成のために細胞質で使用されるアセチル補酵素Aはミトコンドリア起源です:2つのアシルトランスフェラーゼ酵素(1つは細胞質と1つはミトコンドリア)とトランスロカーゼ酵素の作用により、ごく一部がカルニチンを介して輸送されます。アセチルの一部ミトコンドリア起源の補酵素Aは、特殊な経路で得られます。 クエン酸リアーゼ (名前はこのパスの最初の酵素に由来します)。
ミトコンドリアに存在するアセチル補酵素Aは、ピルビン酸デヒドロゲナーゼの作用後の解糖に由来します。アセチル補酵素Aは、クエン酸シンターゼ酵素の作用を受けます。この酵素は、アセチル補酵素Aとオキサロ酢酸との反応によってクエン酸の形成を触媒します。クレブス回路がエネルギー需要を満たすことができる場合、クエン酸回路の一部(クレブス回路に不要な量)がミトコンドリアを離れて細胞質に到達し、そこでエネルギーを消費するクエン酸リアーゼ酵素がそれをアセチル補酵素Aに変換します。このようにして、アセチル補酵素Aを細胞質で利用できるようにすることは可能ですが、形成されたオキサロ酢酸は、クエン酸シンターゼ酵素で再び利用できるようにするためにミトコンドリアに戻されなければなりません。
次に、オキサロ酢酸は酵素の作用によってリンゴ酸に変換されます リンゴ酸デヒドロゲナーゼ 細胞質(細胞質NADHが消費される):リンゴ酸は透過性代謝物であり、ミトコンドリアに再び入ることができ、ミトコンドリアのリンゴ酸デヒドロゲナーゼ酵素の作用下で、オキサロ酢酸に再変換されます(NADHも得られます)。あるいは、細胞質患者は、脱炭酸および脱水素を実行するリンゴ酸酵素の作用を受けて、ピルビン酸に変換することができる。リンゴ酸酵素はNADP +に作用します(ニコチンアミドアデニンジヌクレオチドに似ていますが、これとは異なり、2つのリボースユニットの1つの2番目のヒドロキシル基にリン酸基があります)。したがって、リンゴ酸からピルビン酸への移行時にNADPHが生成されます(次に、ピルビン酸はミトコンドリアに入り、ピルビン酸カルボキシラーゼの作用によってオキサロ酢酸に変換されるか、ピルビン酸デヒドロゲナーゼを介してアセチル補酵素Aに変換されます。
例を見てみましょう:パルミチン酸(16個の炭素原子を持つ鎖)を合成するには8分子のアセチル補酵素Aが必要ですが、そのように使用されるのはそのうちの1つだけです:7分子のアセチル補酵素Aは「酵素」によってマロニル補酵素Aに変換されます アセチル補酵素Aカルボキシラーゼ (この酵素はCO2分子を使用し、補因子としてビオチンを持っています)。
アセチル補酵素Aカルボキシラーゼ酵素は、ほぼ不活性な分散型と活性な凝集型(約20単位)で存在する可能性があります。分散型から凝集型への移行は、細胞質に「高濃度のクエン酸塩:クエン酸塩はアセチル補酵素Aカルボキシラーゼ酵素の正のモジュレーター。
アセチル補酵素Aカルボキシラーゼ酵素には、他の正(インスリン)および負(グルカゴン、アドレナリン、およびアシル補酵素A)のモジュレーターがあります。
この合成が7つの異なるタンパク質の作用によって起こる大腸菌での脂肪酸の合成を分析します。真核細胞では、脂肪酸の合成が行われるメカニズムは細菌のメカニズムと似ていますが、真核生物では、合成に関与する7つの酵素が2つの多酵素複合体AとBに分類されます。
細菌では、7つの異なる遺伝子が次のことをコードしています。
- ACP(アシルキャリアタンパク質);
- ACP-アセチルトランスアセチラーゼ;
- ACP。マロニルトランスアセチラーゼ;
- β-ケト-アシル-ACPシンターゼ(凝縮酵素);
- β-ケト-アシル-ACPレダクターゼ;
- D-β-ヒドロキシ-アシルデヒドラターゼ;
- enoil-ACPが編集されました。
真核生物では、2つの遺伝子が次のことをコードしています。
サブユニットA
ACP;
凝縮酵素
β-ケト-アシル-ACPレダクターゼ。
サブユニットB
ACP-アセチルトランスアセチラーゼ;
ACP-マロニルトランスアセチラーゼ;
D-β-ヒドロキシ-アシルデヒドラターゼ;
enoil-ACPが編集されました。
大腸菌の7つのタンパク質は、中央のタンパク質(ACP)とその周りに他の6つのタンパク質が存在するように配置されています。
2つのスルフヒドリル基がその酵素作用に関与しています:1つはシステインに属し、もう1つはホスホパンテテインの長腕に属します; ACPは基質に結合し、基質はホスホパンテインアームを介して他の酵素と接触し、酵素作用を実行することができます。
アセチル補酵素A(ACPアセチルトランスアシラーゼによる)はACP酵素(より正確にはシステイン誘導体を形成するシステインの硫黄)に結合し、補酵素Aが放出されます;次にACP-マロニルトランスアシラーゼが介入し、ホスホパンテイン上のマロニル(この過程でも、最初にマロニルに結合していた補酵素Aが放出されます)。
次のステップは、凝縮酵素であるβ-ケト-アシルACPシンターゼを含みます:それは2つの骨格間の融合を可能にします。マロニルは容易に脱炭酸され、アセチル誘導体システインのカルボニルが形成されます:システインが放出され、β-ケト(アセチルアセチル)ホスホパンテチン誘導体が形成されます。
続いて、β-ケト-アシル-ACPレダクターゼが介入し、カルボニルをさらにACP-酵素に還元します(水酸化物はNADPHによって形成され、NADP +に還元されます)。
現在、3-ヒドロキシアシルACPデヒドラターゼが作用し(脱水が起こり)、不飽和系(アルケン)が形成されます。
次のプロセスには、エノイル-ACP-レダクターゼが含まれます(水素化を実行します。アルカンが形成され、NADPHがNADP +に還元されます)。
最後の段階では、最初のサイクルで得られたアシル生成物を、2番目のサイクルを開始できる化合物に変換します。トランスアシラーゼ酵素がアシルをシステインに転移し、パンテチンの部位を解放します。マロニル。
β酸化では、FADの分子を使用して、脱水素化によって不飽和α-β代謝物であるトランスエノイル補酵素Aを取得します。代わりに、脂肪酸の合成では、NADPHの分子を使用して反対の反応を引き起こします。
通常、16個の炭素原子を持つ脂肪酸が合成されますが、18個、22個、または22個の炭素原子を持つ脂肪酸も生成できます。次に、脂肪酸はエステル化されて、活性化されたグリセロール(すなわち、グリセロール3-リン酸)とトリグリセリドを形成します。後者は、酵素の作用によりジヒドロキシアセトンリン酸から得ることができます。 グリセロールリン酸デヒドロゲナーゼ または酵素を介してグリセロールから グリセロールキナーゼ.
合成された脂肪酸は脂肪組織に送られなければなりません。それらは、トリグリセリドの形で、または部分的にはアルブミンである輸送体タンパク質を使用して、血流中で輸送されます。