有効成分:イメクロモン
カンタビリン300mgコーティング錠
なぜカンタビリンが使われるのですか?それはなんのためですか?
カンタビリンには、胆道治療に使用される薬のグループに属する活性物質イメクロモンが含まれています。胆嚢および胆汁産生の障害を治療するために使用されます。
カンタビリンは以下の治療に使用されます:
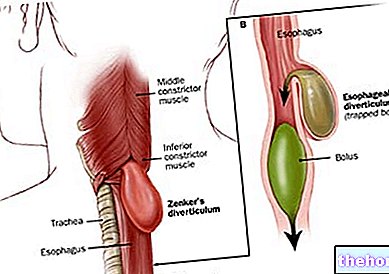
- 胆嚢からの胆汁の流れの障害(胆汁性運動障害)
- 胆汁産生障害によって引き起こされる消化不良(消化不良)
- 胆道のけいれんと胆汁の流出を調節する弁(オッディ括約筋)
カンタビリンは、以下の治療の補助剤としても使用されます。
- 胆嚢の炎症
- 胆石(胆嚢結石症)
- 胆嚢の外科的除去後
- 軽度から中等度の肝機能の問題(軽度から中等度の肝不全)。
カンタビリンを使用すべきでない場合の禁忌
ハイメクロモンまたはこの薬の他の成分のいずれかにアレルギーがある場合
使用上の注意カンタビリンを服用する前に知っておくべきこと
次のような場合は、カンタビリンを服用する前に医師または薬剤師に相談してください。
- 「胆道閉塞
- 重度の肝機能の問題。
どの薬や食品がカンタビリンの効果を変える可能性があるか
他の薬を服用している、最近服用した、または服用する可能性があるかどうかを医師または薬剤師に伝えてください。
警告次のことを知っておくことが重要です。
妊娠、母乳育児、出産
妊娠中または授乳中の方、妊娠中または出産予定の方は、この薬を服用する前に医師または薬剤師に相談してください。
カンタビリンが胎児または授乳中の乳児に及ぼす影響は不明であるため、妊娠中または授乳中にカンタビリンを使用することはお勧めしません。
機械の運転と使用
カンタビリンは、機械を運転したり使用したりする能力には影響しません。
カンタビリンには、サンセットイエロー、ショ糖、ブドウ糖が含まれています。
製品に含まれるもの:
- サンセットイエロー、アレルギー反応を引き起こす可能性のある着色剤
- 液体ブドウ糖およびショ糖;一部の糖分に不耐性があると医師から言われた場合は、この医薬品を服用する前に医師に連絡してください。
投与量、投与方法および投与時間カンタビリンの使用方法:薬
常にこのリーフレットに記載されているとおりに、または医師または薬剤師の指示に従ってこの薬を服用してください。疑わしい場合は、医師または薬剤師に相談してください。推奨用量は、1日2〜3回1〜2錠です。推奨される1日量を超えないようにしてください。
カンタビリンの服用を忘れた場合
忘れた分を補うために2回分を服用しないでください。
この薬の使用についてさらに質問がある場合は、医師または薬剤師に相談してください。
過剰摂取カンタビリンを過剰摂取した場合の対処方法
あなたや他の誰かが誤ってカンタビリン錠を飲みすぎた場合は、医師に相談するか、可能であればパックを持って最寄りの病院に行ってください。
副作用カンタビリンの副作用は何ですか
すべての薬と同様に、この薬は副作用を引き起こす可能性がありますが、誰もがそれらを得るわけではありません。
一般的な副作用(100人に1人から10人に影響する可能性があります):
- 下痢
不明(利用可能なデータから頻度を推定することはできません):
- じんましん、かゆみ、呼吸困難、顔、唇、喉、舌の腫れ(浮腫)などのアナフィラキシー反応。アナフィラキシーショックに進行する可能性があります。
副作用の報告
副作用が出た場合は、医師または薬剤師に相談してください。これには、このリーフレットに記載されていない可能性のある副作用も含まれます。また、国の報告システムwww.agenziafarmaco.it/it/responsabiliを介して直接副作用を報告することもできます。副作用を報告することにより、この薬の安全性に関するより多くの情報を提供するのに役立ちます。
有効期限と保持
この薬は子供の視界や手の届かないところに保管してください。
EXP後のカートンに記載されている有効期限後は、この薬を使用しないでください。有効期限はその月の最終日を指します。
廃水や家庭ごみで薬を捨てないでください。使用しなくなった薬は薬剤師に捨ててください。環境保護に役立ちます。
その他の情報
カンタビリンに含まれるもの
有効成分はイメクロモンです。各錠剤には300mgが含まれています
他の成分は次のとおりです。
コーンスターチ、微結晶性セルロース、アラビアゴム、沈降シリカ、ステアリン酸マグネシウム、タルク、デキストリン、液体グルコース、ショ糖、エリスロシン(E 127)、サンセットイエロー(E 110)、カルナウバワックス。サンセットイエロー、スクロース、グルコースの詳細については、セクション2の終わりを参照してください。
カンタビリンの外観とパックの内容
カンタビリンでコーティングされた錠剤は、30または40錠の水ぶくれに詰められています。すべてのパックサイズが販売されているわけではありません。
ソースパッケージリーフレット:AIFA(イタリア医薬品庁)。 2016年1月に公開されたコンテンツ。現在の情報は最新ではない可能性があります。
最新バージョンにアクセスするには、AIFA(イタリア医薬品庁)のWebサイトにアクセスすることをお勧めします。免責事項と有用な情報。
01.0医薬品の名前
カンタビリン30MGコーティング錠
02.0定性的および定量的組成
1つのコーティングされた錠剤が含まれています: 有効成分: イメクロモン300mg。
賦形剤:液体ブドウ糖、サンセットイエロー(E110)
添加剤の完全なリストについては、セクション6.1を参照してください。
03.0剤形
コーティング錠
04.0臨床情報
04.1治療適応
胆道ジスキネジア。不十分な胆汁産生機能に続発する消化不良。オッディ括約筋と胆道のけいれん。胆嚢結石症、胆嚢炎および胆嚢摘出術の後遺症のアジュバント。中小肝不全のアジュバント。
04.2投与の形態と方法
1日2〜3回コーティングされた1〜2錠。
04.3禁忌
活性物質またはいずれかの賦形剤に対する過敏症。
04.4使用に関する特別な警告と適切な注意事項
胆管の閉塞や重度の肝不全の場合は使用しないでください。この薬には、アレルギー反応を引き起こす可能性のあるアゾ染料であるサンセットイエローが含まれています。
まれなブドウ糖-ガラクトース吸収不良の問題がある患者は、この薬を服用しないでください。
04.5他の医薬品との相互作用および他の形態の相互作用
製品の広範な使用は、他の薬との特定の相互作用を明らかにしませんでした。
04.6妊娠と授乳
妊娠中の女性におけるカンタビリンの使用に関するデータは入手できません。動物実験では催奇形性の影響は示されていません。
予防措置として、妊娠中のカンタビリンの使用を避けることが望ましいです。
ハイメクロモンまたはその代謝物が母乳に排泄されるかどうかは不明です。
04.7機械の運転および使用能力への影響
カンタビリンは、機械を運転したり使用したりする能力には影響しません。
04.8望ましくない影響
各頻度クラス内で、望ましくない影響が重大度の高い順にリストされています。頻度は次のように定義されます:非常に一般的≥1/ 10、一般的≥1/ 100、非一般的≥1/ .1000、および
胃腸障害
共通:下痢
免疫系の障害
不明:アナフィラキシーショックに進行する可能性のある蕁麻疹、そう痒症、呼吸困難、クイック浮腫、低血圧などのアナフィラキシー反応。
疑わしい副作用の報告
医薬品の承認後に発生した疑わしい副作用の報告は、医薬品のベネフィット/リスクバランスを継続的に監視できるため重要です。医療専門家は、国の報告システムを介して疑わしい副作用を報告するよう求められます。 ://www.agenziafarmaco.gov.it/it/responsabili
04.9過剰摂取
過剰摂取の症例は報告されていません
05.0薬理学的特性
05.1薬力学的特性
ATCコード:A05AX02
ハイメクロモンは、元の合成によって再現された天然の有効成分であり、定義上、真の胆汁分泌促進剤ですが、胆嚢、特にオッディ括約筋に対する痙攣作用もあり、他の臓器に対する痙攣作用はありません。二重の好ましい作用機序のおかげで、胆嚢機能全体を回復させます。
-アトロピン効果のない、コリシストおよびオッディ括約筋に対する選択的鎮痙作用。
-コラゴーグ効果のない穏やかで長引く胆汁分泌促進作用。
オッディ括約筋と胆嚢のレベルでの鎮痙作用と胆嚢作用は、胆道の手術中に男性でも確認されています。
05.2薬物動態特性
ハイメクロモンは経口投与後かなり急速に吸収され、2時間以内にピーク血清濃度に達します。明らかに肝親和性であり、肝臓に集中し、そこでグルクロン酸に結合します。胆汁とともに排泄され、その後肝臓に再吸収されます。腸、腸肝サークルを作成します。薬物は主に尿路から排泄されます。
05.3前臨床安全性データ
動物の毒物学的試験では、毒性現象、成長または行動異常、催奇形性または胎児毒性は示されませんでした。実際、急性毒性は非常に低く、経口投与のLD50は7593 mg / Kgです。マウスとラットで6220mg / Kg。犬で800-2400mg / Kg /日を3ヶ月間、ラットで400-1000mg / Kg /日を4ヶ月間長期経口投与すると、「薬の優れた忍容性。
06.0医薬品情報
06.1添加剤
コーンスターチ、微結晶性セルロース、アラビアゴム、沈降シリカ、ステアリン酸マグネシウム、タルク、デキストリン、カルナウバワックス、ショ糖、液体グルコース、エリスロシン(E 127)、サンセットイエロー(E 110)。
06.2非互換性
イメクロモンと他の化合物との化学的・物理的非相溶性は知られていない。
06.3有効期間
5年。
06.4保管に関する特別な注意事項
この医薬品は、特別な保管条件を必要としません。
06.5即時包装の性質および包装の内容
P.V.C.のブリスターとアルミニウム
300mgの30および40のコーティングされた錠剤
06.6使用および取り扱いに関する指示
なし。
07.0マーケティング承認保持者
GR&UUml; NENTHAL ITALIA S.r.l. -カルロボー経由、11-20143ミラノ
08.0マーケティング承認番号
「300mgコーティング錠」、30コーティング錠-A.I.C. NS。 021300013
「300mgコーティング錠」、40コーティング錠-A.I.C. NS。 021300025
09.0最初の承認または承認の更新の日付
初回登録:1970年6月30日
AICの更新:2012年5月
10.0本文の改訂日
2015年7月