現在の疫学データによると、SARS-CoV-2は世界の200か国以上に存在し、世界中で約1億1,300万人がCOVID-19に感染しており(2021年2月)、そのうち250万人は罹患していません。死亡しました。
SARS-CoV-2は主に気道に影響を与えるウイルスで、咳、風邪、発熱、重症の場合は呼吸困難などの症状を引き起こします。ただし、全身性炎症を引き起こし、敗血症、心不全、多臓器不全を引き起こすこともあります。
SARS-CoV-2感染は、60歳以上の人、慢性疾患(例:糖尿病、冠状動脈疾患)、免疫系抑制薬(例:化学療法、免疫抑制剤)で治療を受けている人にとって特に危険です。
この記事は、SARS-CoV-2の構造、ゲノム、タンパク質を分析し、ウイルスの病因に関連する基本的な情報を提供することを目的としています。
詳細情報:SARS-CoV-2:最初の症状を認識する方法と何をすべきか 、SARS-CoV-2は、ペリカプシド(または 封筒).
ペリキャプシドは、いくつかのウイルスのキャプシドの周りに配置される一種のエンベロープです。リン脂質と糖タンパク質で構成されています。
SARS-CoV-2は、9,860アミノ酸をコードする29,881個の窒素塩基のゲノムを持っています。
このゲノムは、構造タンパク質の遺伝子と非構造タンパク質の遺伝子に分けられます。
構造タンパク質遺伝子は、スパイクタンパク質(Sと略記)、ペリカプシドタンパク質(エンベロープからEと略記)、膜タンパク質(Mと略記)、およびヌクレオカプシドタンパク質(Nと略記)をコードします。
名前が示すように、構造タンパク質は結合してSARS-CoV-2の構造を形成します。
一方、非構造タンパク質の遺伝子は、3-キモトリプシンに類似したプロテアーゼ、パパインに類似したプロテアーゼ、またはRNA依存性RNAポリメラーゼなどのタンパク質をコードしており、その機能は複製プロセスを調節および指示しています。ウイルスアセンブリ。
以下は、プロテインSに焦点を当てた、個々の構造タンパク質と非構造タンパク質の説明です。
知ってた ...
SARS-CoV-2は、そのゲノムの約82%をSARS-CoV(SARSの原因)およびMERS-CoV(中東呼吸器症候群の原因)コロナウイルスと共有しています。
詳細情報:コロナウイルス:それらは何ですか? 王冠の外観(したがって、「コロナウイルス」という用語)。
スパイクタンパク質の重量は180〜200 kDa(キロダルトンと読みます)で、1,273個のアミノ酸で構成されています。
スパイクは、S1サブユニット(14-685)およびS2サブユニット(686-1.273)と呼ばれる2つの主要なアミノ酸成分で構成されています。
- S1サブユニットは、RBD(英語の頭字語「受容体結合ドメイン"、すなわち受容体結合ドメイン)、これはウイルスを宿主(すなわちヒト)の細胞に結合するために不可欠である。
- 一方、S2サブユニットはアミノ酸配列(融合ペプチド、HR1、HR2、膜貫通ドメイン、細胞質ドメイン)の部位であり、その最終的な機能は、ウイルスの融合と宿主細胞への侵入を促進することです。
本来の状態(つまり、ウイルスが誰にも感染していないとき)では、スパイクタンパク質は不活性な前駆体の形をしています。しかし、ウイルスが感染する可能性のある生物に遭遇すると、すぐに活性型に切り替わります。標的細胞のプロテアーゼが活性化プロセスをトリガーし(したがって、ウイルスを活性化するのはホスト自体です!)、これが「破壊」します。 S1およびS2サブユニットをスパイクして形成します。
SARS-CoV-2スパイクタンパク質のしくみ

SARS-CoV-2スパイクタンパク質の機能は複雑です。問題の記事は、読者が理解できるように、可能な限り単純化することを目的としています。
スパイクタンパク質は、宿主の感染プロセスを開始するために不可欠です。言い換えると、COVID-19として知られる感染を引き起こすために新規コロナウイルスが使用する武器です。
スパイクによる感染プロセスは、次の2つの段階に分けることができます。
- 宿主細胞への結合。これは、ウイルスが攻撃して生物の細胞に結合し、感染する段階です。
- ウイルス膜(本質的にウイルスの)と宿主細胞の膜との融合。これは、ウイルスが攻撃された生物の細胞に入り、そこでゲノムを広げることを可能にする段階です。
宿主細胞への結合
スパイクタンパク質は、S1サブユニットのRBD配列を介して宿主細胞に結合します。
科学的研究により、RBD配列は「細胞自体の原形質膜の表面に配置されたACE2受容体との相互作用によって」宿主細胞に結合することが観察されています。
ACE2は酵素であり、アンジオテンシン1-9の変換に関与するタンパク質であるACEと相同です。
ヒトでは、ACE2は主に肺、腸、心臓、腎臓などの臓器の細胞の原形質膜の表面に見られます。
S1サブユニットがACE2に結合すると、Sタンパク質はコンフォメーションを変化させ始めます。このイベントは、融合段階とウイルスの宿主細胞への侵入を促進するのに役立ちます。
ACE2への結合とその結果生じるコンフォメーション変化は、SARS-CoV-2に対するワクチンの実現と、宿主によって実施される抗原性と免疫応答のメカニズムを理解するための2つの基本的な側面です。
ただし、考慮しなければならない問題があります。S1サブユニット、特にRBD配列の変異は、コンフォメーション変化の発生方法を変える可能性があります。その結果、これは抗原特性と有効性ワクチンに影響を与える可能性があります(学習するため)このトピックの詳細については、SARS-CoV-2のバリアント専用の記事を読むことをお勧めします。
宿主細胞融合
スパイクタンパク質は、S2サブユニットのアミノ酸配列を介してウイルスを宿主細胞に融合させます。
ウイルス融合プロセスは、RBDと宿主ACE2受容体の間の結合によって誘導されるプロテインSのコンフォメーション変化の波で起こります。スパイクコンフォメーションの変化は、実際、ウイルス膜を宿主細胞の原形質膜に近づけます。 、相互作用まで、膜間の融合まで、そして最後に、感染ウイルスの取り込みまで。
ウイルスゲノムが宿主細胞内に入ると、ウイルスはその複製を開始し、感染プロセスは完了したと見なすことができます。
詳細情報:スパイクタンパク質変異:SARS-CoV-2変異体 成熟し、その核酸(DNAまたはRNA)がキャプシドと呼ばれるタンパク質カプセルに封入されています。この点に関する研究は、SARS-CoV-2プロテインEがビリオンであり、宿主細胞に入ると、ゴルジ装置と小胞体の膜に局在し、集合と放出を促進することを示しています。ビリオンの。
ビロポリンは、宿主の細胞内で膜チャネルとして機能するウイルスタンパク質です。
SARS-CoV-2プロテインEはSARS-CoVと非常に似ていますが、MERS-CoVとはいくつかの違いがあります。
プロテアーゼと呼ばれ、ウイルスによって早期に産生されるウイルス。これらのプロテアーゼは、単一の非構造タンパク質を生成するために、ポリタンパク質を正確なポイントで「切断」します。
ポリプロテイン戦略(より小さなタンパク質が由来する)はウイルスの間で非常に一般的です。
切断作業の前に、ポリタンパク質にまだ含まれているタンパク質は不活性で機能的ではないことを指摘するのは興味深いことです。プロテアーゼの介入と主要アミノ酸鎖に対する切断の後にのみ機能的になります。
SARS-CoV-2非構造タンパク質の主な機能は、ウイルスRNAの転写と複製を処理することです。
ただし、これらのタンパク質はウイルスの病因にも関与していることに注意する必要があります。
SARS-CoV-2プロテアーゼ
SARS-CoV-2の基本となる2つの非構造タンパク質は、間違いなく、ポリタンパク質を「切断」し、ウイルスRNAの転写と複製に有用なタンパク質を形成するプロテアーゼです。
これらのプロテアーゼは、3-キモトリプシン様プロテアーゼ(3CLproと略記)およびパパイン様プロテアーゼ(PLproと略記)として知られています。
それらが生じさせるタンパク質が宿主に感染を広げるのに役立つことを考えると、問題のプロテアーゼは興味深い薬理学的標的を表している。
RNARNA依存性ポリメラーゼ
RNA依存性RNAポリメラーゼは、新しいビリオンに向かうウイルスゲノムの複製に不可欠なSARS-CoV-2の非構造タンパク質です。
この非構造タンパク質は、魅力的な薬理学的標的にもなります。
宿主の複製とそれらを利用して、自身のゲノムをRNAに翻訳し、同じ遺伝物質の複製と新しいビリオンの組み立てに必要なタンパク質を作成します。上記に基づいて、ウイルスRNAの転写と複製における重要な役割は非構造タンパク質に属します。
ウイルスゲノムの転写と複製により、SARS-CoV-2は宿主に広がり始め、実際の感染症を引き起こします。
この段階では、ウイルスは、細胞破壊活性(すなわち、細胞を殺す)と免疫介在性メカニズムの両方で宿主生物に作用します。
細胞破壊活性に関する限り、証拠は、SARS-CoV-2がアポトーシス(細胞死)と細胞溶解を誘発することを示唆しています。より具体的には、ウイルスが感染細胞内でシンシチウムを生成し、細胞破裂を引き起こすことが明らかになりました。 、複製後。
免疫介在性のメカニズムに関しては、SARS-CoV-2が自然免疫系と適応免疫系(抗体とTリンパ球)の両方に関与していることが研究によって示されています。
SARS-CoV-2がSARSコロナウイルスよりも感染性が高いのはなぜですか?
SARSの原因となるコロナウイルスであるSARS-CoVも、RBDと気道の細胞に存在するACE2受容体との相互作用を利用して宿主細胞に侵入します。
ただし、このタイプの結合とSARS-CoV-2によって設定されたものとの間には重要な違いがあります。COVID-19の原因となるコロナウイルスのRBD配列は、ACE2に対してはるかに親和性が高く、はるかに効率的に結合します。 、宿主細胞の侵入過程ではるかに効果的になります。
この点に関する科学的研究は、上記の相互作用の違いは、SARS-CoVのRBDとSARS-CoV-2のRBDの間の異なるアミノ酸組成によるものであることを示しています。特に、重要な違いがある2つのアミノ酸領域があります。
この親和性の違いは、いくつかの側面を説明しています。
- SARS-CoV-2のR0がSARS-CoVよりも高い理由。
- SARS-CoV RBD配列を標的とし、効果的であると思われる薬物およびワクチンがSARS-CoV-2に対して適切でないと思われる理由。
R0とは何ですか?
「基本再生産数」としても知られるR0は、完全に感受性のある集団(つまり、新たに出現する病原体と接触したことがない)の各感染者によって引き起こされた二次感染の平均数を表します。
このパラメータは、感染症の潜在的な伝染性を測定します。
炎症性サイトカインは、免疫系の特定の細胞の活動から発生します。
通常の条件下では、それらは免疫応答、炎症および造血を調節するのに役立ちます。
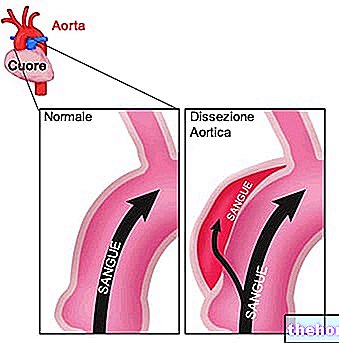
さらに、臨床データおよび他の研究は、重度のSARS-CoV-2感染の存在下で見られる炎症性サイトカインの過剰産生が他の臓器(例えば心臓)に広がり、それらを機能不全にし、凝固に影響を与える可能性があることを示していますプロセス、血栓の形成を誘発します。
SARS-CoV-2が炎症性サイトカインの広範な過剰産生を引き起こす場合、専門家はその現象を「サイトカインストーム症候群」と呼びます。