有効成分:イミペネム、シラスタチン
TIENAM 500 mg / 500mg粉末輸液用
適応症なぜTienamが使用されているのですか?それはなんのためですか?
TIENAMは、カルバペネム系抗生物質と呼ばれる薬のグループに属しています。大人から1歳以上の子供まで、体のさまざまな部分に感染を引き起こすさまざまな細菌(細菌)を殺します。
処理
次の種類の感染症の1つ(または複数)があるため、医師がTIENAMを処方しました。
- 複雑な腹部感染症
- 肺に影響を与える感染症(肺炎)
- 出産中または出産後に発生する可能性のある感染症
- 複雑な尿路感染症
- 複雑な皮膚および軟部組織感染症
TIENAMは、細菌感染が原因であると疑われる発熱がある白血球数の少ない患者の治療に使用できます。
TIENAMは、上記の感染症のいずれかに関連する可能性のある血液の細菌感染症の治療に使用できます。
Tienamを使用すべきでない場合の禁忌
TIENAMは使用しないでください
- イミペネム、シラスタチン、またはTIENAMの他の成分のいずれかにアレルギーがある場合
- ペニシリン、セファロスポリン、カルバペネムなどの他の抗生物質にアレルギーがある場合。
使用上の注意Tienamを服用する前に知っておくべきこと
TIENAMには特に注意してください
あなたが持っている、または持っていた病状についてあなたの医者に伝えてください:
- 抗生物質を含むあらゆる種類の薬に対するアレルギー(即時の治療を必要とする突然の生命を脅かすアレルギー反応)
- 大腸炎またはその他の胃腸疾患
- 腎機能障害を含む、腎臓または尿路に影響を与える問題(腎機能障害のある患者のTIENAMの血中濃度の上昇。用量を腎機能に調整しないと中枢神経系の副作用が発生する可能性があります)
- 限局性振戦や発作(発作)などの中枢神経系障害
- 肝臓の問題。
赤血球を破壊する可能性のある抗体の存在を示す検査(クームス試験)に対して陽性反応を示す可能性があります。あなたの医者はあなたとこれについて話し合います。
バルプロ酸またはバルプロ酸ナトリウムと呼ばれる薬を服用しているかどうかを医師に伝えてください(以下の他の薬との併用を参照)。
子供達
TIENAMは、1歳未満の子供や腎臓に問題のある子供にはお勧めしません。
相互作用どの薬や食品がティエナムの効果を変えることができるか
処方箋なしで入手した薬を含め、他の薬を服用している、または最近服用したことがあるかどうかを医師または薬剤師に伝えてください。
いくつかのウイルス感染症の治療に使用されるガンシクロビルを服用しているかどうかを医師に伝えてください。
また、バルプロ酸またはバルプロ酸ナトリウム(てんかん、双極性障害、片頭痛、統合失調症の治療に使用)またはその他のワルファリンのような抗凝血剤を服用しているかどうかを医師に伝えてください。
TIENAMをこれらの薬と組み合わせて使用するかどうかは医師が決定します。
警告次のことを知っておくことが重要です。
妊娠と母乳育児
TIENAM療法を開始する前に、妊娠中または妊娠を計画している場合は医師に伝えることが重要です。TIENAMは妊娠中の女性では研究されていません。潜在的な利点が潜在的なリスクを正当化すると医師が判断しない限り、妊娠中にTIENAMを使用しないでください。子供の発達。
TIENAM療法を開始する前に、母乳育児をしているのか、母乳育児をするつもりなのかを医師に伝えることが重要です。少量のこの薬が母乳に移行し、その結果、乳児に影響を与える可能性があります。したがって、医師が使用するかどうかを決定します。治療中のTIENAM。授乳時間。
薬を使用する前に、医師または薬剤師にアドバイスを求めてください。
機械の運転と使用
そこにないものを見たり、聞いたり、感じたり、めまい、眠気、めまいを感じたりするなど、この薬に関連するいくつかの副作用があり、運転や機械の使用を妨げる可能性があります(セクション4を参照)。
TIENAMのいくつかの成分に関する重要な情報
低ナトリウム食の患者では、この医薬品には500mgの用量で約1.6mEq(約37.6 mg)のナトリウムが含まれていることを考慮に入れる必要があります。
投与量、投与方法および投与時間Tienamの使用方法:Posology
TIENAMは、医師または他の医療専門家によって準備および管理されます。あなたの医者はあなたが必要とするTIENAMの量を決定します。
大人と青年
成人および青年のTIENAMの通常の投与量は、6時間ごとに500 mg / 500 mg、または6または8時間ごとに1,000 mg / 1,000mgです。腎臓に問題がある場合、または体重が70 kg未満の場合は、医師が投与量を減らす可能性があります。
子供達
1歳以上の子供のための通常の用量は6時間ごとに15/15または25 / 25mg / kgの用量です。 TIENAMは、1歳未満の子供や腎臓に問題のある子供にはお勧めしません。
投与方法
TIENAMは、500 mg / 500 mg以下の用量で投与された場合は20〜30分以上、500 mg / 500 mgを超える用量で投与された場合は40〜60分以上静脈内投与されます。気分が悪くなると、点滴速度が遅くなることがあります。
過剰摂取あなたがあまりにも多くのTienamを服用した場合の対処法
必要以上にTIENAMを使用する場合
過剰摂取の症状には、発作(発作)、錯乱、震え、吐き気、嘔吐、低血圧、心拍数の低下などがあります。 TIENAMの投与量が多すぎると思われる場合は、すぐに医師または他の医療専門家に連絡してください。
TIENAMの使用を忘れた場合
服用していないと思われる場合は、すぐに医師または他の医療専門家に連絡してください。
忘れた分を補うために2回分を服用しないでください。
TIENAMの服用をやめたら
医師の指示があるまで、TIENAMの服用を中止しないでください。
この薬の使用についてさらに質問がある場合は、医師または薬剤師に相談してください。
副作用Tienamの副作用は何ですか
すべての薬と同様に、TIENAMは副作用を引き起こす可能性がありますが、誰もがそれらを得るわけではありません。
以下にリストされている可能性のある副作用の頻度は、次の規則を使用して定義されています。
- 非常に一般的:10人に1人以上のユーザーに影響
- 共通:100人中1〜10人のユーザーに影響します
- 珍しい:1,000人中1〜10人のユーザーに影響
- まれ:10,000人の1〜10人のユーザーに影響します
- 非常にまれ:10,000人に1人未満のユーザーに影響します
- 不明:利用可能なデータから頻度を推定することはできません
以下の副作用はめったに発生しませんが、TIENAMによる治療中または治療後にこれらの副作用が発生した場合は、投与を中止し、直ちに医師に連絡する必要があります。
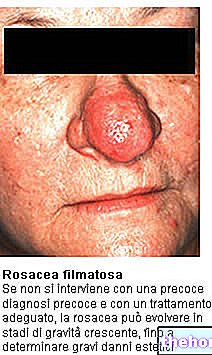
- 皮膚の発疹、顔、唇、舌および/または喉の腫れ(呼吸困難または嚥下困難)、および/または低血圧を含むアレルギー反応
- 皮膚の剥離(中毒性表皮壊死症)
- 重度の皮膚反応(スティーブンスジョンソン症候群および多形紅斑)
- 皮膚や髪の毛の喪失を伴う重度の発疹(剥離性皮膚炎)
その他の考えられる副作用:
一般
- 吐き気、嘔吐、下痢。吐き気と嘔吐は、白血球数が少ない患者でより頻繁に発生するようです
- 触ると非常に痛い静脈に沿った腫れと赤み
- 発疹
- 血液検査で見られる異常な肝機能
- いくつかの種類の白血球の増加
珍しい
- 局所的な皮膚の発赤
- 注射部位の局所的な痛みと硬結
- かゆみを伴う皮膚
- 蕁麻疹
- 熱
- 血液の細胞成分が関与し、通常は血液検査で検出される血液障害(症状は倦怠感、皮膚の蒼白、怪我後の持続的なあざなど)
- 血液検査で見られる腎臓、肝臓、血液機能の変化
- 制御されていない震えと筋肉のけいれん
- 発作(発作)
- 精神障害(気分のむらや判断力の低下など)
- 存在しないものを見たり、聞いたり、感じたりする(幻覚)
- 錯乱
- めまい、眠気
- 低血圧
レア
- 真菌感染症(カンジダ症)
- 歯および/または舌の変色
- 重度の下痢を伴う結腸の炎症
- 味の変化
- 肝臓が正常な機能を発揮できない
- 肝臓の炎症
- 腎臓が正常な機能を発揮できない
- 尿量の変化、尿の色の変化
- 脳疾患、チクチクする感覚、限局性振戦
- 難聴
非常にまれな
- 炎症による肝機能の重度の喪失(劇症肝炎)
- 胃や腸の炎症(胃腸炎)
- 血性下痢(出血性大腸炎)による腸の炎症
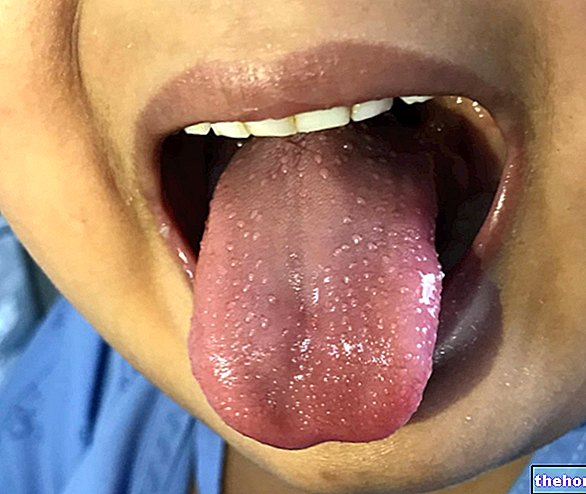
- 赤く腫れた舌、通常舌に見られる突起の過度の成長により、毛深い外観、胸焼け、喉の痛み、唾液産生の増加
- 胃痛
- 回転性(めまい)、頭痛
- 耳鳴り(耳鳴り)
- 多くの関節の痛み、脱力感
- 不整脈、強いまたは速い心拍
- 胸痛、呼吸困難、異常に速く浅い呼吸、脊椎上部の痛み
- 発赤、顔や唇の青色の変色、皮膚組織の変化、過度の発汗
- 女性の外陰部のかゆみ
- 赤血球数の変化
- 筋力低下(重症筋無力症の悪化)に関連するまれな病気の悪化
不明
- 異常な動き
- 攪拌
副作用が深刻になった場合、またはこのリーフレットに記載されていない副作用に気付いた場合は、医師または薬剤師にご相談ください。
有効期限と保持
TIENAMを子供の手の届かないところに置いてください。
パックに記載されている有効期限が切れた後は、TIENAMを使用しないでください。有効期限は、その月の最後の日を指します。
25°C以上で保管しないでください。
再構成後:希釈液はすぐに使用する必要があります。再構成の開始から静脈内注入の終了までの時間間隔は2時間を超えてはなりません。
再構成した溶液を凍結しないでください。
薬は廃水や家庭ごみとして処分しないでください。使用しなくなった薬は薬剤師に捨ててください。環境保護に役立ちます。
組成および剤形
TIENAMに含まれるもの
- 有効成分はイミペネムとシラスタチンです。各バイアルには、500mgのイミペネムに相当するイミペネム一水和物と500mgのシラスタチンに相当するシラスタチンナトリウムが含まれています。
- 賦形剤は重曹です。
TIENAMの外観とパックの内容の説明
TIENAMは、ガラスバイアルに入っている輸液用の白色から淡黄色の粉末です。 1、10、または25バイアルのパック。すべてのパックサイズが販売されているわけではありません。
ソースパッケージリーフレット:AIFA(イタリア医薬品庁)。 2016年1月に公開されたコンテンツ。現在の情報は最新ではない可能性があります。
最新バージョンにアクセスするには、AIFA(イタリア医薬品庁)のWebサイトにアクセスすることをお勧めします。免責事項と有用な情報。
01.0医薬品の名前
点滴用溶液用TIENAM500 MG / 500 MG粉末
02.0定性的および定量的組成
各バイアルには、無水イミペネム500mgに等しいイミペネム一水和物とシラスタチン500mgに等しいシラスタチンナトリウム塩が含まれています。
既知の効果を持つ賦形剤:
各バイアルには、約1.6 mEqのナトリウム(約37.6 mg)に相当する重炭酸ナトリウムが含まれています。
添加剤の完全なリストについては、セクション6.1を参照してください。
03.0剤形
注入のための解決のための粉。
白から淡黄色の粉末。
04.0臨床情報
04.1治療適応
TIENAMは、成人および1歳以上の子供における以下の感染症の治療に適応されます(セクション4.4および5.1を参照)。
•複雑な腹腔内感染症
•院内肺炎および人工呼吸器関連肺炎を含む重度の肺炎
•産褥内および産後の感染症
•複雑な尿路感染症
•複雑な皮膚および軟部組織感染症
TIENAMは、「細菌感染症」の疑いのある発熱性好中球減少症患者の治療に使用できます。
上記の感染症のいずれかに関連して発生する、または関連する疑いのある細菌血症の患者の治療。
抗菌剤の適切な使用に関する公式ガイドラインを検討する必要があります。
04.2投与の形態と方法
投与量
TIENAMの推奨用量は、投与するイミペネム/シラスタチンの量を表しています。
TIENAMの1日量は、感染の種類に応じて決定し、病原体の感受性と患者の腎機能の評価によって決定される均等に分割された用量で投与する必要があります(セクション4.4および5.1も参照)。
大人と青年
腎機能が正常な患者(クレアチニンクリアランス≥90ml/分)の場合、推奨用量は次のとおりです。
6時間ごとに500mg / 500mgまたは
1,000 mg / 1,000 mg8時間ごとまたは6時間ごと
感受性の低い細菌種( 緑膿菌)および非常に重度の感染症(例:発熱を伴う好中球減少症の患者)は、6時間ごとに1,000mg / 1,000mgを投与して治療されます。
クレアチニンクリアランスが
最大総1日量は4,000mg / 4,000mg /日を超えてはなりません。
腎機能障害
腎機能障害のある成人の減量の決定:
1. 1日の総投与量(例:2,000 / 2,000、3,000 / 3,000または4,000 / 4,000 mg)を選択し、通常は腎機能が正常な患者に適用する必要があります。
2.表1から、患者のクレアチニンクリアランスに基づいて適切な減量が選択されます。注入時間については、を参照してください 投与方法.
表1
クレアチニンクリアランスのある患者
これらの患者は、血液透析が48時間以内に行われない限り、TIENAMを投与すべきではありません。
血液透析を受けている患者
クレアチニンクリアランスのある患者を治療する場合
イミペネムとシラスタチンの両方が血液透析中に循環から排除されます。患者は、血液透析後および血液透析治療の終了後12時間にTIENAMを投与する必要があります。透析中の患者、特に中枢神経系(CNS)疾患の根底にある患者は、注意深く監視する必要があります。血液透析患者の場合、TIENAMは、利益が発作の潜在的なリスクを上回る場合にのみ推奨されます(セクション4.4を参照)。
現在、腹膜透析患者にTIENAMの使用を推奨するにはデータが不十分です。
肝機能障害
肝機能障害のある患者には用量調整は推奨されません(セクション5.2を参照)。
高齢者人口
腎機能が正常な高齢患者では、用量調整は必要ありません(セクション5.2を参照)。
小児人口 1歳以上
1歳以上の小児患者の場合、推奨用量は6時間ごとに投与される15/15または25/25 mg / kgの用量です。
感受性の低い細菌種( 緑膿菌)および非常に重度の感染症(例:発熱を伴う好中球減少症の患者)は、6時間ごとに25/25 mg / kgを投与して治療されます。
小児人口
臨床データは、1歳未満の子供への投与を推奨するには不十分です。
腎機能障害のある小児集団
腎機能障害(血清クレアチニン> 2 mg / dl)の小児患者への投与を推奨するには、臨床データが不十分です。セクション4.4を参照してください。
投与方法
TIENAMは、投与前に再構成してから希釈する必要があります(セクション6.2、6.3、および6.6を参照)。 500 mg / 500 mg以下の各用量は、20〜30分かけて静脈内注入することによって投与する必要があります。 500 mg / 500 mgを超える各用量は、40〜60分の期間にわたって注入する必要があります。点滴中に吐き気がする患者では、点滴の速度が遅くなることがあります。
04.3禁忌
•活性物質またはセクション6.1に記載されている賦形剤のいずれかに対する過敏症。
•他のカルバペネム系抗菌剤に対する過敏症。
•他のタイプのベータラクタム抗菌剤(ペニシリンやセファロスポリンなど)に対する重度の過敏症(アナフィラキシー反応、重度の皮膚反応など)。
04.4使用に関する特別な警告と適切な注意事項
全般的
患者を治療するためのイミペネム/シラスタチンの選択は、感染の重症度、他の適切な抗菌剤に対する耐性の有病率、および耐性細菌を選択するリスクなどの要因に基づいて、カルバペネム抗菌剤の使用の適切性を考慮する必要がありますカルバペネムに。
過敏症
ベータラクタム系抗生物質を投与されている患者では、重篤で時折致命的な過敏症(アナフィラキシー)反応が報告されています。これらの反応の発症は、複数のアレルゲンに対する過敏症の病歴のある被験者でより頻繁でした。TIENAMによる治療を開始する前に、カルバペネム、ペニシリン、セファロスポリン、その他のベータラクタムおよびその他のアレルゲンに対する以前の過敏反応に特に注意を払う必要があります(を参照)。セクション4.3)TIENAMに対するアレルギー反応を直ちに停止する必要がある場合深刻なアナフィラキシー反応には、即時の緊急治療が必要です。
肝臓
肝毒性(トランスアミナーゼの増加、肝不全、劇症肝炎など)のリスクがあるため、イミペネム/シラスタチンによる治療中は肝機能を注意深く監視する必要があります。
肝疾患の患者での使用:既存の肝障害のある患者は、イミペネム/シラスタチンによる治療中に肝機能のモニタリングを受ける必要があります。用量調整は必要ありません(セクション4.2を参照)。
血液学
イミペネム/シラスタチンによる治療中に、陽性の直接的または間接的なクームス試験が発生する可能性があります。
抗菌スペクトル
経験的治療を開始する前に、特に生命を脅かす病気では、イミペネム/シラスタチンの抗菌スペクトルを考慮する必要があります。さらに、皮膚や軟部組織の感染症などに関連する特定の病原体のイミペメン/シラスタチンに対する感受性が限られているため、注意が必要です。イミペネム/シラスタチンの使用は、病原体がすでに文書化されており、感受性が高いことが判明していない限り、または最も可能性の高い病原体が治療に感受性があるという高い疑いがない限り、このタイプの感染症の治療には適していません。 -メチシリン耐性菌 黄色ブドウ球菌 (MRSA)は、MRSA感染が疑われるか、承認された適応症に関与していることが証明された場合に適応となる可能性があります。承認された適応症に関与している疑いがある、または文書化されている場合 緑膿菌 アミノグリコシドの併用が適応となる場合があります(セクション4.1を参照)。
バルプロ酸との相互作用
イミペネム/シラスタチンとバルプロ酸/バルプロ酸ナトリウムの併用は推奨されていません(セクション4.5を参照)。
クロストリジウム・ディフィシル
抗生物質関連大腸炎および偽膜性大腸炎は、イミペネム/シラスタチンおよび事実上他のすべての抗菌剤で報告されており、重症度は軽度から生命を脅かすものまでさまざまです。イミペネム/シラスタチンの使用と同時にまたは使用後に下痢を発症する患者では、この診断を考慮することが重要です(セクション4.8を参照)。イミペネム/シラスタチン療法の中断および特定の治療の実施を検討する必要があります。 クロストリジウム・ディフィシル。 蠕動を阻害する医薬品は投与しないでください。
髄膜炎
TIENAMは髄膜炎の治療には推奨されません。
腎機能障害
イミペネム/シラスタチンは、腎機能障害のある患者に蓄積します。用量が腎機能に調整されていない場合、CNSの副作用が発生する可能性があります。このセクションのセクション4.2および4.4「中枢神経系」を参照してください。
中枢神経系
ミオクローヌス活動、混乱状態、発作などの中枢神経系の副作用が報告されており、特に腎機能と体重に基づいて処方された投与量を超えた場合に報告されています。これらの影響は、CNS障害(脳損傷や発作の既往など)のある患者、および/または投与された物質の蓄積が発生する可能性のある腎機能障害のある患者でより頻繁に報告されています。したがって、特にこれらの患者では、推奨される投与量を注意深く遵守することが主張されます(セクション4.2を参照)。てんかん性障害が知られている患者では、抗けいれん療法を継続する必要があります。
発作の危険因子がわかっている小児の神経学的症状または発作、または発作の閾値を下げる医薬品との併用治療には特に注意を払う必要があります。
限局性振戦、ミオクローヌス、または発作が発生した場合、患者は神経学的に評価され、まだ確立されていない場合は抗けいれん療法を受ける必要があります。 CNS症状が続く場合は、TIENAMの投与量を減らすか中止する必要があります。
クレアチニンクリアランスのある患者
小児人口
臨床データは、1歳未満の患者または腎機能障害のある小児患者(血清クレアチニン> 2 mg / dl)でのTIENAMの使用を推奨するには不十分です。上記も参照してください。 中枢神経系.
TIENAM 500 mg / 500 mgには、37.6 mgのナトリウム(1.6 mEq)が含まれています。これは、管理されたナトリウム食を摂取している患者で考慮する必要があります。
04.5他の医薬品との相互作用および他の形態の相互作用
ガンシクロビルとTIENAMで治療された患者で全身性発作が報告されています。これらの医薬品は、潜在的な利益がリスクを上回らない限り、治療に組み合わせるべきではありません。
バルプロ酸がカルバペネム剤と同時投与された場合、治療範囲を下回る可能性のある血清バルプロ酸の減少が報告されています。
バルプロ酸の血清レベルが低下すると、発作の制御が不十分になる可能性があります。したがって、イミペネムとバルプロ酸/バルプロ酸ナトリウムの併用は推奨されておらず、代替の抗菌または抗けいれん療法を検討する必要があります(セクション4.4を参照)。
経口抗凝固薬
抗生物質とワルファリンの同時投与は、その抗凝固効果を高める可能性があります。抗菌剤との併用療法を受けている患者におけるワルファリンを含む、経口投与された抗凝固剤の抗凝固効果の増加に関する多くの報告があります。リスクは、基礎となる感染症、年齢、患者の一般的な健康状態によって異なる可能性があるため、INR(国際標準化比率)の増加に対する抗生物質の寄与を評価することは困難です。患者を監視することをお勧めします。 。抗生物質と経口抗凝固剤の同時投与中および投与直後に頻繁にINR。
TIENAMとプロベネシドの同時投与は、血漿レベルとイミペネムの半減期の最小限の増加をもたらしました。イミペネムをプロベネシドと併用した場合、活性(代謝されていない)イミペネムの尿中回復は用量の約60%減少しました。TIENAMとプロベネシドの同時投与は2倍になりました。シラスタチンの血漿レベルと半減期は、シラスタチンの尿中回復に影響を与えませんでした。
小児人口
相互作用の研究は成人でのみ実施されています。
04.6妊娠と母乳育児
妊娠
妊娠中の女性におけるイミペネム/シラスタチンの使用に関する適切で十分に管理された研究はありません。
妊娠中のサルを対象とした研究では、生殖毒性が示されています(セクション5.3を参照)。人間の潜在的なリスクは不明です。
TIENAMは、潜在的な利益が胎児への潜在的なリスクを正当化する場合にのみ、妊娠中に使用する必要があります。
えさの時間
イミペネムとシラスタチンは母乳中に少量排泄されます。経口投与後、両方の成分の吸収が制限されます。したがって、授乳中の乳児がかなりの量にさらされる可能性は低いです。 TIENAMの使用が必要であると考えられる場合、子供にとっての母乳育児の利点は、起こりうるリスクと比較検討されなければなりません。
受胎能力
男性または女性の出産に対するイミペネム/シラスタチン治療の潜在的な影響に関する利用可能なデータはありません。
04.7機械の運転および使用能力への影響
機械の運転や使用能力への影響に関する研究は行われていませんが、一部の患者の運転能力やめまいに影響を与える可能性のある、薬に関連するいくつかの望ましくない影響(幻覚、めまい、傾眠、めまいなど)があります。使用機械(セクション4.8を参照)。
04.8望ましくない影響
イミペネム/シラスタチンの静脈内投与で治療された1,723人の患者の臨床試験で、少なくとも治療に関連している可能性があると報告された最も頻繁な全身性副作用は、悪心(2.0%)、下痢(1.8%)、嘔吐(1.5%)、発疹( 0.9%)、発熱(0.5%)、低血圧(0.4%)、けいれん(0.4%)(セクション4.4を参照)、めまい(0.3%)、かゆみ(0.3%)、ハイブ(0.2%)、眠気(0.2%) 。同様に、最も頻繁に報告された局所副作用は、静脈炎/血栓性静脈炎(3.1%)、注射部位の痛み(0.7%)、注射部位の紅斑(0.4%)、および静脈硬結(0.2%)でした。血清トランスアミナーゼおよびアルカリホスファターゼの上昇が一般的に報告されています。
以下の副作用は、臨床試験および医薬品の商業的使用中に報告されました。
すべての副作用は、システムの臓器クラスと頻度によって報告されます:非常に一般的(≥1/ 10)。一般的(≥1/ 100、
各周波数グループ内で、望ましくない影響が重大度の降順でリストされています。
小児人口 (3ヶ月以上)
生後3か月以上の178人の小児患者を対象とした研究では、報告された副作用は成人で報告されたものと一致していました。
疑わしい副作用の報告
医薬品の承認後に発生した疑わしい副作用の報告は、医薬品のベネフィット/リスクバランスを継続的に監視できるため重要です。医療専門家は、国の報告システムを介して疑わしい副作用を報告するよう求められます。 //www.aifa.gov.it/content/segnalazioni-reazioni-avverse。
04.9過剰摂取
発生する可能性のある過剰摂取の症状は、副作用プロファイルと一致しています。これらには、けいれん、混乱、震え、吐き気、嘔吐、低血圧、徐脈が含まれる場合があります。 TIENAMによる過剰摂取の治療に関する情報はありません。イミペネム/シラスタチンナトリウムは血液透析可能です。ただし、過剰摂取の場合のこの手順の有用性は知られていません。
05.0薬理学的特性
05.1薬力学的特性
薬物療法グループ:全身使用のための抗菌剤、カルバペネム。
ATCコード:J01DH51。
作用機序
TIENAMには、イミペネムとシラスタチンナトリウムの2つの成分が1:1の重量比で含まれています。
N-ホルムイミドイルチエナマイシンとしても識別されるイミペネムは、糸状菌によって生成される元の化合物であるチエナマイシンの半合成誘導体です。 Streptomycescattleya。
イミペネムは、ペニシリン結合タンパク質(PBP)に結合することにより、グラム陽性菌およびグラム陰性菌の細菌細胞壁の合成を阻害することにより、殺菌活性を発揮します。
シラスタチンナトリウムは、イミペネムを代謝および不活性化する腎酵素であるデヒドロペプチダーゼ-Iの競合的で可逆的かつ特異的な阻害剤です。固有の抗菌作用はなく、イミペネムの抗菌作用には影響しません。
薬物動態/薬力学(FC / FD)の関係
他のベータラクタム抗菌剤と同様に、イミペネム濃度が最小発育阻止濃度(MIC)(T> MIC)を超える時間は、有効性とよりよく相関することが示されています。
抵抗メカニズム
イミペネムに対する耐性は、以下の原因による可能性があります。
•グラム陰性菌の外膜の透過性の低下(ポリンの生成の低下による)
•イミペネムは排出ポンプでセルから積極的に取り除くことができます
•ペニシリン結合タンパク質(PBPS)のイミペネムに対する親和性の低下
•イミペネムは、カルバペネムを加水分解する比較的まれなベータラクタマーゼを除いて、グラム陽性菌およびグラム陰性菌によって産生されるペニシリナーゼおよびセファロスポリナーゼを含むほとんどのベータラクタマーゼに対して加水分解に対して安定です。他のカルバペネムに対する耐性種は一般に共を示します。イミペネムに対する耐性イミペネムと、キノロン、マクロライドアミノグリコシドおよびテトラサイクリンのクラスに属する薬剤との間に、標的に基づく交差耐性はありません。
ブレークポイント
感受性(S)病原体と耐性(R)病原体を区別するためのイミペネムのEUCAST MICブレークポイントは次のとおりです(v 1.1 2010-04-27)。
• Enterobacteriaceae1: S≤2mg/ l、R> 8 mg / l
• 緑膿菌属2: S≤4mg/ l、R> 8 mg / l
• アシネトバクター属: S≤2mg/ l、R> 8 mg / l
• ブドウ球菌属3: セフォキシチン感受性から推測
• エンテロコッカス属: S≤4mg/ l、R> 8 mg / l
• 連鎖球菌A、B、C、G: のベータラクタマーゼに対する感受性 連鎖球菌 溶血性ベータA、B、C、およびGは、ペニシリン感受性から推測されます
• Streptococcus pneumoniae4: S≤2mg/ l、R> 2 mg / l
•その他の連鎖球菌4:S≤2mg/ l、R> 2 mg / l
• インフルエンザ菌4:S≤2mg/ l、R> 2 mg / l
• Moraxella catarrhalis4: NS。 ≤ 2 mg / l, R> 2 mg / l
• ナイセリア淋菌: の証拠が不十分です ナイセリア淋菌 イミペネム療法の良いターゲットです
•グラム陽性嫌気性菌:S≤2mg/ l、R> 8 mg / l
•グラム陰性嫌気性菌:S≤2mg/ l、R> 8 mg / l
•種に関連しないブレークポイント5:S≤2mg/ l、R> 8 mg / l
1 プロテウスおよびモルガン菌属 imipenemの次善のターゲットと見なされます。
2のブレークポイント シュードモナス 高用量を頻繁に投与する治療法を参照してください(6時間ごとに1g)。
3ブドウ球菌のカルバペネムに対する感受性は、セフォキシチンに対する感受性から推測されます。
感受性ブレークポイントを超えるMIC値を持つ4株は非常にまれであるか、まだ報告されていません。これらの分離株のそれぞれについて、同定と抗菌薬感受性試験を繰り返し、結果が確認された場合、分離株を参照検査室に送る必要があります。現在の耐性ブレークポイントよりも大きいMICが確認された分離株の臨床反応の証拠が得られるまで、耐性があると報告されています。
5種に関連しないブレークポイントは、主にFC / FDデータから決定され、特定の種のMIC分布とは無関係です。これらは、種に関連するブレークポイントの概要または注記に記載されていない種にのみ使用する必要があります。
感度
後天性耐性の有病率は地理的にも時間とともに変化する可能性があり、特に重度の感染症を治療する場合は、耐性に関する地域情報が望ましい。必要に応じて、耐性の局所的な有病率が、少なくともいくつかのタイプの感染症における薬剤の有用性が疑わしいようなものである場合、専門家の助言を求めるべきである。
*すべてのメチシリン耐性ブドウ球菌はイミペネム/シラスタチンに耐性があります。
**種に関連しないEUCASTブレークポイントが使用されます。
05.2「薬物動態特性
イミペネム
吸収
健康なボランティアでは、20分以上続くTIENAM注入により、250 mg / 250 mgの用量で12〜20 mcg / ml、500 mgの用量で21〜58 mcg / mlの範囲のイミペネムのピーク血漿レベルが得られました。 / 500 mg、および1,000 mg / 1,000 mgの用量で41〜83 mcg /ml。250mg/ 250 mg、500 mg / 500 mg、および1,000 mg / 1,000mgの用量でのイミペネムの平均ピーク血漿レベルは17でした。 、39、および66 mcg / mL。これらの用量では、イミペネムの血漿レベルは4〜6時間で1 mcg / mL以下に低下します。
分布
イミペネムの血清タンパク質への結合は約20%です。
生体内変化
単独で投与されると、イミペネムはデヒドロペプチダーゼ-Iによって腎臓で代謝されます。いくつかの研究では、個々の尿の回収率は5〜40%の範囲であり、平均回収率は15〜20%でした。
シラスタチンは酵素デヒドロペプチダーゼIの特異的阻害剤であり、イミペネムの代謝を効果的に阻害するため、イミペネムとシラスタチンの併用投与により、尿と血漿の両方でイミペネムの治療抗菌レベルに到達することができます。
排除
イミペネムの血漿中半減期は1時間でした。投与された抗生物質の約70%が10時間以内に尿中に変化せず、薬物のそれ以上の尿中排泄は検出されませんでした。イミペネムの尿中濃度は、TIENAM 500 mg / 500後最大8時間10mcg / mlを超えたままでした。投与された用量の残りは、抗菌的に不活性な代謝物の形で尿中に回収され、イミペネムの糞便中排泄は本質的にゼロでした。
腎機能が正常な患者に6時間ごとにTIENAMを投与したところ、血漿または尿中のイミペネムの蓄積は観察されませんでした。
シラスタチン
吸収
TIENAMの20分間注入後のシラスタチンのピーク血漿レベルは、250 mg / 250 mg用量あたり21〜26 mcg / mL、500 mg / 500 mg用量あたり21〜55 mcg / mL、および56〜88 mcg / mL /の範囲でした。 1,000mg / 1,000mgの用量。 250 mg / 250 mg、500 mg / 500 mg、および1,000 mg / 1,000 mgの投与後のシラスタチンの平均ピーク血漿レベルは、それぞれ22、42、および72 mcg / mlでした。
分布
シラスタチンの血清タンパク結合は約40%です。
生体内変化と排泄
シラスタチンの血漿中半減期は約1時間です。 TIENAM投与後10時間以内に、シラスタチン投与量の約70〜80%がそのまま尿中にシラスタチンとして回収された後、尿中には回収されなくなり、約10%がN-アセチル代謝物として回収されました。腎臓におけるデヒドロペプチダーゼ-Iの活性は、血流からシラスタチンが除去された直後に正常レベルに戻ります。
特別な集団における薬物動態
腎不全
TIENAM 250 mg / 250 mgの単回静脈内投与後、イミペネムの曲線下面積(AUC)は、軽度(クレアチニンクリアランス(CC)50)の被験者でそれぞれ1.1倍、1.9倍、2.7倍に増加しました。 -80 ml / min / 1.73 m2)、中等度(CC 30-2)、および重度(CC 2)の腎機能障害、正常な腎機能(CC> 80 ml / min / 1.73 m2)の被験者と比較して、AUCはシラスタチンは、正常な腎機能を持つ被験者と比較して、軽度、中等度、および重度の腎機能障害のある被験者で、それぞれ1.6倍、2.0倍、および6.2倍増加しました。血液透析の24時間後に投与されたTIENAM250 mg / 250 mgの単回静脈内投与後、イミペネムとシラスタチンのAUCは、正常な腎機能を持つ被験者よりも、それぞれ3.7倍と16.4倍高かった。イミペネムとシラスタチンの尿中回復、腎クリアランス、血漿クリアランスは、TIENAMの静脈内投与後の腎機能の低下とともに低下します。腎機能障害のある患者では、用量調整が必要です(セクション4.2を参照)。
肝不全
肝不全患者におけるイミペネムの薬物動態は決定されていません。イミペネムの薬物動態の肝臓代謝は限られているため、肝機能障害の影響を受けるとは予想されていません。したがって、肝機能障害のある患者には用量調整は推奨されません(セクション4.2を参照)。
小児人口
イミペネムの平均クリアランス(CL)と分布容積(Vdss)は、成人よりも小児患者(3か月から14歳)で約45%高かった。小児患者に15 / 15mg / kg体重のイミペネム/シラスタチンを投与した後のイミペネムのAUCは、500 mg / 500 mgの用量で治療された成人の曝露よりも約30%高かった。 / 25 mg / kgイミペネム/シラスタチンの小児への曝露は、1,000 mg / 1,000 mgの用量で治療された成人の曝露よりも約9%高かった。
高齢者
健康な高齢ボランティア(65〜75歳で、年齢に応じて正常な腎機能を有する)では、20分以上静脈内投与されたTIENAM 500 mg / 500 mgの単回投与の薬物動態は、軽度の腎機能障害のある被験者で予想されたものと一致していました。用量調整が必要でないと考えられる人。イミペネムとシラスタチンの平均血漿半減期は、それぞれ91±7.0分と69±15分でした。複数回投与しても、イミペネムまたはシラスタチンの薬物動態に影響はなく、イミペネム/シラスタチンの蓄積は観察されませんでした(セクションを参照)。 4.2)。
05.3前臨床安全性データ
非臨床データは、反復投与毒性および遺伝子毒性研究に基づいて、ヒトに対する特別なリスクを明らかにしませんでした。
動物実験では、イミペネムが単一の実体として生成する毒性は腎臓に限定されていることが示されています。シラスタチンとイミペネムを1:1の比率で同時投与すると、ウサギとサルの腎毒性の発症が防止されました。入手可能なデータによると、シラスタチンは、イミペネムが尿細管細胞に侵入するのを防ぐことにより、腎毒性を防ぎます。
イミペネムシラスタチンナトリウムを40 / 40mg / kg /日(静脈内ボーラス)の用量で治療した妊娠中のカニクイザルで実施された奇形学研究は、嘔吐、食欲不振、体重減少、下痢、流産、およびいくつかの死亡例を含む母体毒性を明らかにしました。イミペネムシラスタチンナトリウムの用量(約100/100 mg / kg /日または通常の推奨されるヒトの1日あたりの静脈内投与量の約3倍)を妊娠中のカニクイザルに、「男性」の診療所で使用されているのと同様の静脈内注入速度で投与した場合、最小限の母体不耐性(時折の嘔吐)があり、母体の死亡、催奇形性の証拠はありませんでしたが、対照群と比較して「胚喪失の増加がありました」(セクション4.6を参照)。
イミペネム/シラスタチンの発がん性を評価するための動物での長期試験は実施されていません。
06.0医薬品情報
06.1添加剤
重炭酸ナトリウム。
06.2非互換性
この医薬品は、乳酸と化学的に不適合であり、乳酸を含む希釈剤で再構成してはなりません。しかしながら、それは、乳酸溶液が投与された静脈内注入システムに投与することができる。
この医薬品は、セクション6.6に記載されているものを除き、他の医薬品と混合してはなりません。
06.3有効期間
2年。
再構成後:
希釈液はすぐに使用してください。再構成の開始から静脈内注入の終了までの時間間隔は2時間を超えてはなりません。
06.4保管に関する特別な注意事項
25°C以上で保管しないでください。
再構成した溶液を凍結しないでください。
医薬品の再構成後の保管条件については、セクション6.3を参照してください。
06.5即時包装の性質および包装の内容
20mlのタイプIガラスバイアル。
この薬は、1バイアル、10バイアル、25バイアルのパックで提供されます。
すべてのパックサイズが販売されているわけではありません。
06.6使用および取り扱いに関する指示
各バイアルは使い捨てです。
再構成:
各バイアルの内容物を100mlの適切な注入溶液(セクション6.2および6.3を参照)に移す必要があります:0.9%塩化ナトリウム。臨床上の理由で0.9%塩化ナトリウムを使用できない例外的な状況では、代わりに5%グルコースを使用する必要があります。
推奨される手順は、適切な注入溶液約10 mlをバイアルに追加することです。よく振って、得られた混合物を注入容器の溶液に移します。
注意:混合物を直接注入に使用してはなりません。
注入用の溶液にバイアルの内容物が完全に移動するように、注入用の溶液をさらに10ml使用して繰り返します。得られた混合物は、透明になるまで攪拌する必要があります。
上記の手順に従って再構成された溶液の濃度は、イミペネムとシラスタチンの両方で約5 mg / mlです。
無色から黄色への色の変化は、薬の効力に影響を与えません。
未使用の薬またはこの薬に由来する廃棄物は、地域の規制に従って処分する必要があります。
07.0マーケティング承認保持者
MSD Italia S.r.l.
Vitorchiano経由、151-00189ローマ
08.0マーケティング承認番号
AICn。 025887062
09.0最初の承認または承認の更新の日付
最初の承認日:2011年6月4日
10.0本文の改訂日
2016年1月