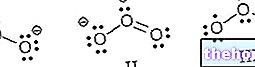
(英語のテキストから自由に翻訳)
生物学的薬剤とは何ですか?
生物学的薬剤は、生物によって生成された、または生物に由来する活性物質を含む薬です。 「例えば、インスリンは、遺伝子組換え技術のおかげでこのホルモンの合成に必要なDNAを発現する生物(真菌や細菌など)によって現在合成されているため、事実上生物学的薬剤です。」
バイオシミラーとは何ですか?
バイオシミラー薬は、その主題に関して管轄機関によってすでに市場で認可されている生物学的薬を特徴付けるものと非常に類似した有効成分を含む薬です。このため、一般的に、2つの薬は同じ病気を治療するために同じ用量で使用されます。同一ではないにしても、同様の成分、および有効成分の名前もあります。
これらすべての類似性にもかかわらず、どちらか一方の薬を服用するかどうかの決定は、医師のみに委ねられています。実際、適応症や副作用がわずかに異なる場合があり、一方の薬の使用が他方よりも適しています。
バイオシミラーの販売承認はどのような基準に基づいていますか?
すべての医薬品と同様に、バイオシミラー医薬品も購入可能になる前に「販売承認」が必要です。この承認は、医薬品の有効性、安全性、品質に関する一連の研究を評価した後、EMEAなどの競争機関によって発行されます。 。
革新的な医薬品は、一定期間、競争からの保護を享受します。この期間が過ぎると、他の製薬会社はバイオシミラーの販売許可を取得することができます。
バイオシミラーはどのように評価されますか?
バイオシミラーが販売される日を考えると、生物学的参照薬はすでに数年前から使用されており、「この点に関して重要な量の研究と情報があります。したがって、これ以上長い必要はありません。評価プロセス。それにもかかわらず、主題に関する立法府が、使用の有効性と安全性に関して有意差がないことを明確に実証する一連の研究を要求している場合でも。さらに、治療の適応症が異なる場合、バイオシミラーの使用の有効性と安全性も、治療される新しい障害または疾患を参照して実証されなければなりません。
これらの厳密な研究に加えて、この主題に関する管轄機関は、他のすべての医薬品と同じ品質基準を尊重してバイオシミラー医薬品を製造することを要求しています。明らかに、この意味でさえ、主題に施行されている法律の遵守についての正確で定期的なチェックの欠如はありません。
バイオシミラーの安全性はどのように監視されていますか?
同様の医薬品を含むすべての医薬品の安全性は、販売承認後も引き続き注意深く監視されています。特に法律では、すべての製薬会社が、免疫学的性質の応答を含め、販売された新薬の安全性監視システムを備えている必要があります。可能性のあるアレルギー現象)明らかに、この場合でも、管轄機関は、この監視システムが現在の法律で要求されている基準に準拠していることを確認します。
このページで公開されているバイオシミラーに関する情報は、古くなっているか、不完全である可能性があります。この情報の正しい使用法については、免責事項と有用な情報のページを参照してください。








.jpg)









.jpg)