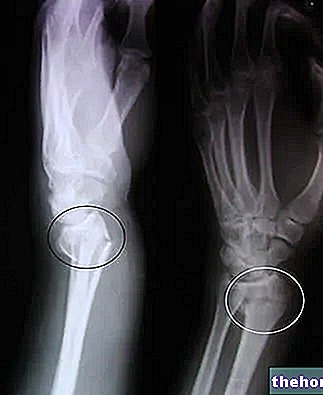
有効成分:クリンダマイシン
ダラシンC150mgハードカプセル
ダラシンC300mgハードカプセル
なぜダラシンcが使用されるのですか?それはなんのためですか?
薬物療法のカテゴリー
全身抗生物質。
治療上の適応症
DALACIN Cカプセルは、感受性嫌気性菌による重度の感染症の治療、およびブドウ球菌、連鎖球菌、肺炎球菌による重度の感染症の治療に適応されます。
DALACIN Cカプセルは、他の抗生物質に耐性のブドウ球菌によって引き起こされる感染症の治療に有効であることが示されています。ただし、クリンダマイシンに耐性のブドウ球菌の菌株が分離されているため、この抗生物質による治療中に感度テストを実行する必要があります。
経口クリンダマイシンは、クラミジア・トラコマチスによる婦人科および骨盤の感染症に、すでに静脈内投与された被験者の維持療法としてのみ使用できます。
クリンダマイシンは、免疫不全患者の日和見トキソプラズマ感染症およびニューモシスチスジロベチ感染症の治療にも効果的です。
クリンダマイシンの使用は、ペニシリンにアレルギーのある患者、または医師の判断でペニシリンが適応とされていない患者のために予約する必要があります。
薬は必要に応じて他の抗生物質と一緒に投与することができます。
重度の大腸炎の発症の可能性を考慮して、医師は、DALACIN Cカプセルによる治療を開始する前に、治療する感染症の性質に関連して、代替として毒性の低い薬剤を使用する可能性を慎重に評価する必要があります。
ダラシンを使用すべきでない場合の禁忌c
クリンダマイシンは、クリンダマイシン、リンコマイシン、またはこの医薬品の他の成分のいずれかに以前に感受性を示した患者には禁忌です。
えさの時間。
ダラシンCは、下痢または炎症性腸疾患の患者に投与してはなりません(特別な警告のセクションを参照)。
使用上の注意ダラシンcを服用する前に知っておくべきこと
これまでに入手可能なデータは、高齢者および/または重病患者が下痢にあまり耐えられないことを示しています。これらの患者がクリンダマイシンで治療される場合、排便の頻度の変化に特に注意を払う必要があります。
DALACIN Cカプセルは、胃腸疾患、特に大腸炎の病歴のある人、およびアトピーの人に注意して処方する必要があります。
抗生物質を使用すると、耐性菌、特に酵母菌が発生することがあります。重感染が発生した場合は、適切な治療措置を講じてください。長期治療中は、定期的な肝臓と腎臓の機能検査と血球計算を行う必要があります。
肝臓と腎臓の機能障害
肝腎症患者では、薬剤の半減期がわずかに変化しただけであるため、軽度から中等度の肝機能障害および腎機能障害の場合、通常、用量を減らす必要はありません。薬の機能肝臓と腎臓長期治療の場合は、肝臓と腎臓の機能検査を実施する必要があります。
脳脊髄液ではクリンダマイシンの有意なレベルに達していないため、髄膜炎の治療にこの薬を使用しないでください。
妊娠中の女性におけるダラシンCの使用に関するデータは限られているため、厳密に必要な場合にのみ使用する必要があります(セクション:出産、妊娠、授乳を参照)。
相互作用どの薬物または食品がダラシンcの効果を変更できるか
最近、処方箋のない薬でも、他の薬を服用したことがある場合は、医師または薬剤師に伝えてください。
血液を薄くするために使用されるワルファリンまたは同様の薬。出血のリスクが高くなる可能性があります。あなたの医者はあなたの血液が凝固する能力をチェックするために定期的な血液検査を受ける必要があるかもしれません。
クリンダマイシンは、他の神経筋遮断薬(エーテル、ツボクラリン、パンクロニウムなど)の活性を高める可能性のある神経筋遮断薬を誘発することが示されています。したがって、このような薬を服用している患者には注意して使用する必要があります。
バクテロイデスフラジリスに対するメトロニダゾールとの相乗作用が報告されています。
ゲンタマイシンとの関連は、相乗作用を決定することがあり、拮抗作用を決定することはありません。
クリンダマイシンとリンコマイシンの交差反応性が実証されています。
クリンダマイシンとエリスロマイシンの間のinvitro拮抗作用が実証されているため、臨床的関連性がある可能性があるため、2つの医薬品を同時に投与しないでください。
HIV陽性の志願者へのクリンダマイシンとプリマキンの投与は、ジドブジンの薬物動態パラメーターに有意な影響を与えませんでした。
一部の抗生物質は経口避妊薬の効果を低下させる可能性があります。治療中は追加の避妊予防策を検討する必要があります。
警告次のことを知っておくことが重要です。
糖分に対する不耐性が確認された場合は、薬を服用する前に医師に連絡してください。
抗生物質による治療は、結腸の正常な細菌叢を変化させ、クロストリジウム・ディフィシルの異常増殖を引き起こします。これは、クリンダマイシンを含むほぼすべての抗生物質の使用で報告されています。クロストリジウム・ディフィシルは、クロストリジウム・ディフィシル関連下痢(CDAD)の発症に寄与する毒素AおよびBを産生し、抗生物質誘発性大腸炎の主な原因です。注意深い病歴抗生物質投与後2か月以上経過しても、クロストリジウム・ディフィシル関連の下痢の症例が報告されているため、これも必要です。
抗生物質投与後に下痢を呈する患者では、CDADの診断を考慮することが重要です。偽膜性大腸炎(「望ましくない影響」のセクションを参照)を含む大腸炎に進行する可能性があり、その重症度は軽度から致命的な大腸炎までさまざまです。大腸炎は通常、腹部のけいれんを伴う重度で持続性の下痢を特徴とし、便中に血液や粘液が存在する場合があります。診断と治療を迅速に行わないと、大腸炎は腹膜炎、ショック、中毒性巨大結腸症に進行する可能性があります。内視鏡検査で偽膜性大腸炎が明らかになることがあります。大腸炎が疑われる場合は、直腸S状結腸鏡検査が推奨されます。大腸炎の存在は、選択培地でのクロストリジウム・ディフィシルの検便および毒素検査によってさらに確認できます。クロストリジウム・ディフィシル。抗生物質による下痢または抗生物質による大腸炎が疑われるか確認された場合は、クリンダマイシンを含む抗生物質による継続的な治療を中止し、適切な治療措置を直ちに講じる必要があります。この状況では、蠕動を阻害する薬は禁忌です。
抗蠕動薬、アヘン剤、ジフェノキシレートとアトロピンは、状態を延長および/または悪化させる可能性があります。
バンコマイシンは、クロストリジウム・ディフィシルによって産生される抗生物質依存性偽膜性大腸炎の治療に有効であることが見出されました。成人の投与量は、7〜10日間で3〜4回のバンコマイシン経口投与で500mg〜2g /日です。
コレスチラミンはinvitroで毒素に結合しますが、この樹脂はバンコマイシンにも結合します。したがって、コレスチラミンとバンコマイシンを同時に投与する場合は、各薬剤を異なる時間に投与することをお勧めします。
バンコマイシンによる治療後に再発するいくつかのまれな症例が報告されています。
出産、妊娠、母乳育児
薬を服用する前に、医師または薬剤師にアドバイスを求めてください。
妊娠
経口および皮下投与後にラットおよびウサギで実施された生殖毒性試験では、母体毒性を誘発する用量を除いて、クリンダマイシンによって引き起こされる出産障害または胎児への危害の兆候は示されていません。動物での生殖研究は、必ずしもヒトでの反応を予測するものではありません。
ヒトでは、クリンダマイシンは胎盤を通過します。反復投与後、羊水濃度は母体血中濃度の約30%でした。
妊娠中の女性を対象とした臨床試験では、第2および第3トリメスターでのクリンダマイシンの全身投与は、先天性異常の頻度の増加とは関連していませんでした。妊娠初期の女性を対象とした適切で十分に管理された研究はありません。
妊娠中、クリンダマイシンは厳密に必要な場合にのみ使用する必要があります。
えさの時間
経口および非経口投与されたクリンダマイシンは、0.7から3.8μg/ mlの範囲の濃度で母乳に含まれています。乳児に深刻な副作用が生じる可能性があるため、授乳中の女性はクリンダマイシンを服用しないでください。
受胎能力
経口クリンダマイシンで治療されたラットの出産する研究は、出産するか生殖能力に影響を与えなかった。
機械を運転して使用する能力への影響
クリンダマイシンは、機械を運転して使用する能力にまったくまたは無視できる影響を及ぼします。
いくつかの成分に関する重要な情報:
薬には乳糖が含まれています。医師から「糖分に不耐性がある」と言われた場合は、この医薬品を服用する前に医師に連絡してください。
投与量と使用方法ダラシンcの使用方法:投与量
小児集団:感染の重症度に応じて、8〜20 mg / kg /日を3回または4回の投与に分けます。
成人:感染の重症度に応じて、600〜1200mg /日を3回または4回の投与に分けます。
婦人科および骨盤感染症の維持療法では、静脈内投与後、6時間ごとに450mgを10〜14日間投与します。
脳トキソプラズマ症:免疫不全患者の場合:2週間6時間ごとに600〜1200 mg、続いて8〜10週間のコースが完了するまで6時間ごとに300〜600mg。
クリンダマイシンをピリメタミンと組み合わせる場合、後者の用量は25〜75 mgを8〜10週間経口投与します。ピリメタミンの用量を増やす場合は、10〜20 mg /日のフォリン酸を投与することをお勧めします。
免疫不全患者におけるニューモシスチスジロベチ肺炎:21日間6時間ごとに300〜450 mg、21日間1日1回経口投与される15〜30mgのプリマキン。
食道への刺激を避けるために、DALACINCカプセルはコップ1杯の水で飲み込む必要があります。
注:ベータ溶血性連鎖球菌感染症の場合、リウマチ熱または糸球体腎炎の可能性を減らすために、少なくとも10日間治療を継続することをお勧めします。
過剰摂取ダラシンcを飲みすぎた場合の対処方法
用量に関連する副作用がないため、特に薬剤が指示どおりに投与された場合、過剰摂取はまれな問題です。
血液透析および腹膜透析は、血清からクリンダマイシンを除去するのに効果的ではありません。
副作用ダラシンcの副作用は何ですか
次の表は、臨床試験と市販後調査から特定された副作用を、システムの臓器クラスと頻度でソートして示しています。市販後の経験から特定された副作用はイタリック体で示されています。頻度グループは、次の規則を使用して定義されます:非常に一般的(≥1/ 10);一般的(≥1/ 100、
パッケージリーフレットに含まれている指示に準拠することで、望ましくない影響のリスクを軽減できます。
副作用の報告
副作用が出た場合は、医師または薬剤師に相談してください。これには、このリーフレットに記載されていない可能性のある副作用も含まれます。望ましくない影響は、www.agenziafarmaco.gov.it / it / responsabiliの全国報告システムを介して直接報告することもできます。副作用を報告することにより、この薬の安全性に関する詳細情報を提供することができます。
有効期限と保持
有効期限:パッケージに印刷されている有効期限を確認してください。
表示されている有効期限は、正しく保管された無傷のパッケージに入った製品を指します。
警告:パッケージに記載されている有効期限が切れた後は、薬を使用しないでください。
25°C以上で保管しないでください。
劣化の明らかな兆候がある場合は使用しないでください。
薬は廃水や家庭ごみとして処分しないでください。使用しなくなった薬は薬剤師に捨ててください。環境保護に役立ちます。
この薬は子供の視界や手の届かないところに保管してください。
締め切り ">その他の情報
構成
ダラシンC150mgハードカプセル
各カプセルには以下が含まれます:
- 有効成分:塩酸クリンダマイシン162.86mg(クリンダマイシンベース150mgに相当)。
- 賦形剤:ステアリン酸マグネシウム、タルク、コーンスターチ、乳糖一水和物。
- カプセルの成分:二酸化チタン、ゼラチン。
ダラシンC300mgハードカプセル
各カプセルには以下が含まれます:
- 有効成分:塩酸クリンダマイシン325.8mg(クリンダマイシンベース300mg相当)。
- 賦形剤:ステアリン酸マグネシウム、タルク、コーンスターチ、乳糖一水和物。
- カプセルの成分:二酸化チタン、ゼラチン。
剤形と内容
ハードカプセル-経口使用
ダラシンC150mgハードカプセル-12カプセル
ダラシンC300mgハードカプセル-24カプセル
ソースパッケージリーフレット:AIFA(イタリア医薬品庁)。 2016年1月に公開されたコンテンツ。現在の情報は最新ではない可能性があります。
最新バージョンにアクセスするには、AIFA(イタリア医薬品庁)のWebサイトにアクセスすることをお勧めします。免責事項と有用な情報。
01.0医薬品の名前-
ダラシンC150MGハードカプセル
02.0定性的および定量的組成-
ダラシンC150mgハードカプセル
各ハードカプセルには次のものが含まれています。
有効成分:塩酸クリンダマイシン162.86mg(クリンダマイシンベース150mgに相当)。
既知の効果を持つ賦形剤:乳糖。
添加剤の完全なリストについては、セクション6.1を参照してください。
03.0剤形-
ハードカプセル。
04.0臨床情報-
04.1治療適応症-
DALACIN Cカプセルは、感受性嫌気性菌による重度の感染症の治療、およびブドウ球菌、連鎖球菌、肺炎球菌による重度の感染症の治療に適応されます。
DALACIN Cカプセルは、他の抗生物質に耐性のブドウ球菌によって引き起こされる感染症の治療に有効であることが示されています。ただし、クリンダマイシンに耐性のブドウ球菌の菌株が分離されているため、この抗生物質による治療中に感度テストを実行する必要があります。
経口クリンダマイシンは、婦人科および骨盤の感染症に使用できます クラミジア・トラコマチス すでに静脈内投与された被験者の維持療法としてのみ。
クリンダマイシンは、からの日和見感染症の治療に効果的です トキソプラズマ原虫 と ニューモシスチスジロベチ 免疫不全の患者で。
クリンダマイシンの使用は、ペニシリンにアレルギーのある患者、またはペニシリンが医師によって指示されていない患者のために予約する必要があります。
薬は必要に応じて他の抗生物質と一緒に投与することができます。
重度の大腸炎の発症の可能性を考慮して、医師は、DALACIN Cカプセルによる治療を開始する前に、治療する感染症の性質に関連して、代替として毒性の低い薬剤を使用する可能性を慎重に評価する必要があります。
04.2投与の形態と方法-
投与量
小児人口
感染の重症度に応じて、8〜20 mg / kg /日を3回または4回の投与に分けます。
大人
感染の重症度に応じて、600〜1200mg /日を3回または4回の投与に分けます。
婦人科および骨盤感染症の維持療法では、静脈内投与後、6時間ごとに450mgを10〜14日間投与します。
免疫不全患者の脳トキソプラズマ症:2週間6時間ごとに600-1200 mg、続いて8-10週間のコースが完了するまで6時間ごとに300-600mg。
クリンダマイシンをピリメタミンと組み合わせる場合、後者の用量は25〜75 mgを8〜10週間経口投与します。ピリメタミンの用量を増やす場合は、10〜20 mg /日のフォリン酸を投与することをお勧めします。
からの肺炎 ニューモシスチスジロベチ 免疫不全患者の場合:21日間6時間ごとに300〜450 mg、21日間1日1回経口投与される15〜30mgのプリマキン。
食道への刺激を避けるために、DALACINCカプセルはコップ1杯の水で飲み込む必要があります。
注:ベータ溶血性連鎖球菌感染症の場合、リウマチ熱または糸球体腎炎の可能性を減らすために、少なくとも10日間治療を継続することをお勧めします。
04.3禁忌-
クリンダマイシンは、以前に活性物質、リンコマイシン、セクション6.1に記載されている賦形剤のいずれかに対して過敏症を示した患者には禁忌です。
えさの時間。
DALACIN Cは、下痢または炎症性腸疾患の患者に投与してはなりません(セクション4.4を参照)。
04.4使用に関する特別な警告と適切な注意事項-
クリンダマイシン療法を受けている患者では、好酸球増加症や全身症状を伴う薬剤反応(DRESS)、スティーブンス・ジョンソン症候群(SJS)、中毒性表皮壊死症(NET)、発疹性膿疱症などの重度の皮膚反応を含む重篤な過敏反応が報告されています。 )。過敏反応または重度の皮膚反応が発生した場合は、クリンダマイシンによる治療を中止し、適切な治療を開始する必要があります(セクション4.3および4.8を参照)。
抗生物質による治療は、結腸の正常な植物相を変化させ、 クロストリジウム・ディフィシル。これは、クリンダマイシンを含むほぼすべての抗生物質の使用で報告されています クロストリジウム・ディフィシル 関連する下痢の発症に寄与する毒素AおよびBを生成します クロストリジウム・ディフィシル (CDAD)そして「抗生物質誘発性大腸炎」の主な原因です。下痢に伴う下痢の症例があるため、注意深い病歴も必要です。 C.難しい それらはまた抗生物質投与後2ヶ月以上報告されています。
抗生物質投与後に下痢を呈する患者では、CDADの診断を考慮することが重要です。偽膜性大腸炎(セクション4.8を参照)を含む大腸炎に進行する可能性があり、その重症度は軽度から致命的な大腸炎までさまざまです。大腸炎は通常、腹部のけいれんを伴う重度で持続性の下痢を特徴とし、便中に血液や粘液が存在する場合があります。診断と治療を迅速に行わないと、大腸炎は腹膜炎、ショック、中毒性巨大結腸症に進行する可能性があります。内視鏡検査で偽膜性大腸炎が明らかになることがあります。大腸炎が疑われる場合は、直腸S状結腸鏡検査をお勧めします。大腸炎の存在は、便培養検査でさらに確認できます。 クロストリジウム・ディフィシル 選択培地および毒素アッセイによる クロストリジウム・ディフィシル。抗生物質による下痢または抗生物質による大腸炎が疑われるか確認された場合は、クリンダマイシンを含む抗生物質による継続的な治療を中止し、適切な治療措置を直ちに講じる必要があります。この状況では、蠕動を阻害する薬は禁忌です。
抗蠕動薬、アヘン剤、ジフェノキシレートとアトロピンは、状態を延長および/または悪化させる可能性があります。
バンコマイシンは、抗生物質依存性偽膜性腸炎の治療に有効であることがわかりました。 クロストリジウム・ディフィシル。成人の投与量は、7〜10日間で3〜4回のバンコマイシン経口投与で500mg〜2g /日です。
コレスチラミンは毒素に結合します 試験管内で:ただし、この樹脂はバンコマイシンにも結合します。したがって、コレスチラミンとバンコマイシンを同時に投与する場合は、各薬剤を異なる時間に投与することをお勧めします。
バンコマイシンによる治療後に再発するいくつかのまれな症例が報告されています。
これまでに入手可能なデータは、高齢者および/または重病患者が下痢にあまり耐えられないことを示しています。これらの患者がクリンダマイシンで治療される場合、排便の頻度の変化に特に注意を払う必要があります。
DALACIN Cカプセルは、胃腸疾患、特に大腸炎の病歴のある人、およびアトピーの人に注意して処方する必要があります。
抗生物質を使用すると、耐性菌、特に酵母菌が発生することがあります。重感染が発生した場合は、適切な治療措置を講じてください。長期治療中は、定期的な肝臓と腎臓の機能検査と血球計算を行う必要があります。
肝臓と腎臓の機能障害
肝腎症患者では、薬剤の半減期がわずかに変化しただけであるため、軽度から中等度の肝機能障害および腎機能障害の場合、通常、用量を減らす必要はありません。薬の機能肝臓と腎臓長期治療の場合は、肝臓と腎臓の機能検査を実施する必要があります。
脳脊髄液ではクリンダマイシンの有意なレベルに達していないため、髄膜炎の治療にこの薬を使用しないでください。
妊娠中の女性におけるダラシンCの使用に関するデータは限られているため、厳密に必要な場合にのみ使用する必要があります(セクション4.6を参照)。
いくつかの成分に関する重要な情報:
薬には乳糖が含まれています。ガラクトース不耐症、ラクターゼ欠乏症、またはブドウ糖-ガラクトース吸収不良のまれな遺伝的問題のある患者は、この薬を服用しないでください。
04.5他の医薬品との相互作用および他の形態の相互作用-
ビタミンK拮抗薬
クリンダマイシンをビタミンK拮抗薬(ワルファリン、アセノクマロール、フルインジオンなど)と組み合わせて治療した患者では、凝固検査(PT / INR)および/または出血の増加が報告されています。したがって、ビタミンK拮抗薬で治療された患者の凝固検査は、頻繁に監視する必要があります。
注射されたクリンダマイシンは、他の神経筋遮断薬(例えば、エーテル、ツボクラリン、パンクロニウム)の活性を高める可能性のある神経筋遮断を誘発することが示されています。したがって、そのような薬を服用している患者には注意して使用する必要があります。
メトロニダゾールとの相乗作用が報告されています バクテロイデスフラジリス.
ゲンタマイシンとの関連は、相乗作用を決定することがあり、拮抗作用を決定することはありません。
クリンダマイシンとリンコマイシンの交差反応性が実証されています。
クリンダマイシンとエリスロマイシンの間のinvitro拮抗作用が実証されているため、臨床的関連性がある可能性があるため、2つの医薬品を同時に投与しないでください。
HIV陽性の志願者へのクリンダマイシンとプリマキンの投与は、ジドブジンの薬物動態パラメーターに有意な影響を与えませんでした。
一部の抗生物質は経口避妊薬の効果を低下させる可能性があります。治療中は追加の避妊予防策を検討する必要があります。
04.6妊娠と母乳育児-
妊娠
経口および皮下投与後にラットおよびウサギで実施された生殖毒性試験では、母体毒性を誘発する用量を除いて、クリンダマイシンによって引き起こされる出産障害または胎児への危害の兆候は示されていません。動物での生殖研究は、必ずしもヒトでの反応を予測するものではありません。
ヒトでは、クリンダマイシンは胎盤を通過します。反復投与後、羊水濃度は母体血中濃度の約30%でした。
妊娠中の女性を対象とした臨床試験では、第2および第3トリメスターでのクリンダマイシンの全身投与は、先天性異常の頻度の増加とは関連していませんでした。妊娠初期の女性を対象とした適切で十分に管理された研究はありません。
妊娠中、クリンダマイシンは厳密に必要な場合にのみ使用する必要があります。
えさの時間
経口および非経口投与されたクリンダマイシンは、0.7から3.8μg/ mlの範囲の濃度で母乳に含まれています。乳児に深刻な副作用が生じる可能性があるため、授乳中の女性はクリンダマイシンを服用しないでください。
受胎能力
経口クリンダマイシンで治療されたラットの出産する研究は、出産するか生殖能力に影響を与えなかった。
04.7機械の運転および使用能力への影響-
クリンダマイシンは、機械を運転して使用する能力にまったくまたは無視できる影響を及ぼします。
04.8望ましくない影響-
次の表は、臨床試験と市販後調査から特定された副作用を、システムの臓器クラスと頻度でソートして示しています。周波数グループは、次の規則に従って定義されます。非常に一般的(≥1/ 10)。一般的(≥1/ 100、
*市販後の経験で特定された副作用。
疑わしい副作用の報告
医薬品の承認後に発生した疑わしい副作用の報告は、医薬品のベネフィット/リスク比の継続的なモニタリングを可能にするため、重要です。
医療専門家は、www.agenziafarmaco.gov.it / it / responsabiliの全国報告システムを介して疑わしい副作用を報告するように求められます。
04.9過剰摂取-
用量に関連する副作用がないため、特に薬剤が指示どおりに投与された場合、過剰摂取はまれな問題です。
血液透析および腹膜透析は、血清からクリンダマイシンを除去するのに効果的ではありません。
05.0薬理学的特性-
05.1「薬力学的特性-
薬物療法グループ:全身使用のための抗菌剤-リンコサミド。
ATCコード:J01FF01。
DALACIN Cカプセルには、リンコマイシン分子の7-ヒドロキシル基の塩素原子で置換することによって得られる半合成抗生物質である塩酸クリンダマイシンが含まれています。
微生物学的活性:クリンダマイシンには「活性」があります 試験管内で 以下の微生物の分離株に対して:
好気性グラム陽性球菌、以下を含む:
黄色ブドウ球菌, 表皮ブドウ球菌 (ペニシリナーゼ産生株を含む)。もともとエリスロマイシンに耐性のあるブドウ球菌のいくつかの菌株をinvitroで試験すると、クリンダマイシン、連鎖球菌( S.フェカリス)、肺炎球菌、 クラミジア・トラコマチス (敏感な株)。
グラム陰性嫌気性桿菌、以下を含む:
バクテロイデス属、フソバクテリウム属。
好気性グラム陽性嫌気性桿菌。
プロピオニバクテリウム、ユーバクテリウム、放線菌属。
以下を含むグラム陽性嫌気性および微好気性球菌:
ペプトコッカス属、ペプトストレプトコッカス属、微好気性連鎖球菌。
クロストリジウム: クロストリジウム菌は、ほとんどの嫌気性菌よりもクリンダマイシンに対して耐性があります。ほとんど ウェルシュ菌 それらは敏感ですが、他の種、例えば私は C.スポロゲネス との C.tertium、クリンダマイシンに耐性があることが多い。感度テストをお勧めします。クリンダマイシンとリンコマイシンの交差耐性、および拮抗作用が実証されています 試験管内で クリンダマイシンとエリスロマイシンの間なので、同時に投与しないでください。
原生動物:
トキソプラズマ原虫、ニューモシスチス・ジロベチ
05.2「薬物動態特性-
健康なボランティア(24人の成人被験者)で実施された薬物動態研究は、150mgの塩酸クリンダマイシンの用量の経口投与後、薬物が急速に吸収されることを示しました。 45分で2.50mcg / mLの平均ピーク血清が達成されました。 3時間後と6時間後の平均血清レベルはそれぞれ1.51mcg / mlと0.70mcg / mlでした。
吸収
経口投与後の吸収は実質的に完了しており(90%)、同時に食物を摂取しても血清濃度はそれほど変化しません。血中濃度は均一で、すべての被験者とさまざまな用量で予測可能でした。 DALACIN Cカプセルを最大14日間繰り返し投与しても、薬物代謝の蓄積や変化は見られませんでした。血液透析および腹膜透析は、血清からクリンダマイシンを除去するのに効果的ではありません。
クリンダマイシンの血清濃度は、投与量の増加とともに直線的に増加し、示された治療用量の投与後少なくとも6時間、ほとんどの示された生物のMIC(最小発育阻止濃度)を超えます。
分布
クリンダマイシンは、体液や組織(骨組織を含む)に広く分布しています。平均半減期は2.4時間です。
排除
薬物の約10%が生物学的に活性な形で尿中に排泄され、3.6%が糞便中に排泄されます。残りは生物不活性代謝物の形で排泄されます。
HIV陽性の志願者へのクリンダマイシンとプリマキンの投与は、ジドブジンの薬物動態パラメーターに有意な影響を与えませんでした。
母乳には、クリンダマイシンが0.7〜3.8 mcg / mlの量で含まれています。
05.3前臨床安全性データ-
実験動物に関する急性毒性データは以下のとおりです。
スパルタスプレーグドーリーラットおよびビーグル犬に30〜100および300mg / kg /日(犬の場合は3g /日)の用量で1年間経口投与された塩酸クリンダマイシンは十分に許容された。
組織病理学的検査は、薬物で治療された動物のグループと対照との間の有意差を明らかにしなかった。
イヌでは胃腸毒性症状(嘔吐、食欲不振および体重減少)が観察されたが、OSあたり6ヶ月間投与された600mg / kg /日の用量はラットによって十分に許容された。
ラットへの製品の経口投与後の胚胎児発生試験、およびラットとウサギへの製品の皮下投与後の胚胎児発生試験では、母体毒性を引き起こす用量を除いて、発生毒性は観察されなかった。
06.0医薬品情報-
06.1添加剤-
ステアリン酸マグネシウム、タルク、コーンスターチ、乳糖一水和物;
カプセル成分:二酸化チタン、ゼラチン。
06.2非互換性 "-
関係ありません。
06.3有効期間 "-
5年。
06.4保管に関する特別な注意事項-
25°C以上で保管しないでください。
06.5即時包装の性質と包装の内容-
透明なPVCとアルミニウムを組み合わせたブリスター。ヒートシールペイントでラッカー塗装されています。
「ダラシンC150mgハードカプセル」12カプセル。
06.6使用と取り扱いの説明-
未使用の薬やこの薬に由来する廃棄物は、地域の規制に従って処分する必要があります。
07.0「マーケティング承認」の保有者-
ファイザーイタリアS.r.l.
Isonzo経由、71-04100ラティーナ(LT)
08.0マーケティング承認番号-
022633059「ダラシンC150mgハードカプセル」12カプセル
09.0最初の承認または承認の更新の日付-
最初の承認日:1973年11月23日
最新の更新日:2010年5月31日
10.0テキストの改訂日-
2016年5月23日








.jpg)