ガーダシルとは何ですか?
ガーダシルは、4種類のヒトパピローマウイルス(6、11、16、18型)の精製タンパク質を含む注射用懸濁液からなるワクチンです。バイアルまたはプレフィルドシリンジで利用できます。
ガーダシルは何に使用されますか?
ガーダシルは、9歳以上の患者に次の症状から保護するために使用されます。
- 特定の癌性タイプのヒトパピローマウイルス(HPV)によって引き起こされる、生殖器領域(子宮頸部、外陰部、または膣)の前癌病変(異常な細胞増殖)および子宮頸癌。
- 特定の種類のHPVによって引き起こされる外性器疣贅(性器疣贅)。
ガーダシルは公式の推奨に従って投与されます。
ワクチンは処方箋がなければ入手できません。
ガーダシルはどのように使用されていますか?
ガーダシルは、1回目と2回目の投与の間に2か月の間隔で、2回目と3回目の投与の間に4か月の間隔で、3回の投与で少なくとも9歳の人々に与えられます。別のスケジュールが必要な場合は、2回目の投与は最初の投与の少なくとも1か月後に、3回目の投与は2回目の投与の少なくとも3か月後に行う必要があります。すべての用量は1年以内に投与する必要があります。ガーダシルの最初の投与を受けたら、3回すべての投与を行うことで治療を完了することをお勧めします。ワクチンは、筋肉、できれば肩や太ももに注射することで投与されます。
ガーダシルはどのように機能しますか?
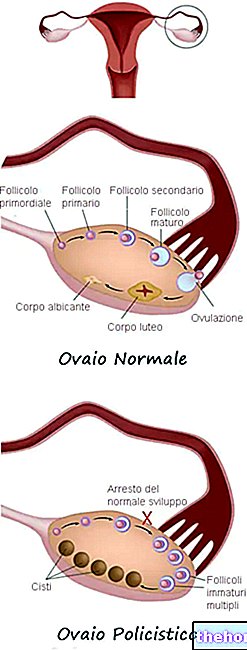
パピローマウイルスは、いぼや異常な組織成長を引き起こすウイルスです。パピローマウイルスには100種類以上あり、そのうちのいくつかは性器の癌に関連しています。 HPVタイプ16および18は子宮頸がんの約70%の原因であり、HPVタイプ6および11は生殖器疣贅の約90%を引き起こします。
すべてのパピローマウイルスには、「L1タンパク質」と呼ばれるタンパク質で構成されたエンベロープまたは「キャプシド」があります。ガーダシルには、HPVタイプ6、11、16、18用の精製L1タンパク質が含まれています。これらは、「組換えDNA技術」として知られる方法で生産されます。つまり、L1タンパク質を生成できる遺伝子(DNA)を受け取った酵母によって生産されます。タンパク質は「ウイルス様粒子」(つまり、HPVウイルスに似た構造であるため、体がそれらを認識するのに問題がない)に収集され、感染を引き起こすことはできません。
患者がワクチンを接種すると、免疫系はL1タンパク質に対する抗体を産生します。ワクチン接種後、免疫系は実際のウイルスにさらされたときに抗体をより迅速に生成することができます。これは、これらのウイルスによって引き起こされる病気から保護するのに役立ちます。
ワクチンには、より良い反応を刺激する「アジュバント」(アルミニウムを含む化合物)も含まれています。
ガーダシルはどのように研究されてきましたか?
ガーダシルは、16歳から26歳までの合計約21,000人の女性を対象とした4つの主要な研究で研究されています。ガーダシルはプラセボ(ダミーワクチン)と比較されました。この研究では、HPV感染に起因する性器の病変またはいぼを発症した女性の数を調べました。研究参加者は、ワクチンの3回目の投与後約3年間観察されました。
追加の研究では、24〜45歳の約4,000人の女性を対象にHPVタイプ6、11、16、18および関連する生殖器病変の感染を予防するGardasilの能力を調べ、これらのタイプのHPVに対する抗体の発生を約1,700人の少女と少年で観察しました。 9と15。
研究中にGardasilはどのような利点を示しましたか?
ガーダシルは、子宮頸部、外陰部、膣の前癌性生殖器病変、子宮頸がん、およびタイプ6、11、16、18のHPV関連疣贅に対して有効でした。
4つの研究すべての結果を一緒に見ると、過去に「HPVタイプ6、11、16、または18の感染症にかかったことがない」ガーダシルのワクチン接種を受けた8,000人以上の女性のうち、1人が子宮頸部に前癌病変を発症しました。対照的に、ワクチンとしてプラセボを投与された8,000人を超える女性のうち85人は、これらのタイプのHPVに起因する病変を持っていました。分析に他の2種類のHPV(タイプ6および11)による子宮頸部病変も含まれている場合、Gardasilの同様の効果が見られました。
HPVタイプ6、11、16または18に起因する外性器病変(疣贅および外陰部または膣の前癌病変を含む)に関して、実施された3つの研究の結果を一緒に調べた。ガーダシルグループの約8,000人の女性のうち2人が性器いぼを発症しましたが、外陰部または膣の前癌病変の報告はありませんでした。対照的に、プラセボ群では、約8,000人の女性で合計189例の外性器病変が検出されました。
研究はまた、ガーダシルが、31型を含む他の癌性タイプのHPVに関連する子宮頸部病変に対してある程度の保護を提供することを示しました。
追加の研究により、24〜45歳の女性のHPV損傷および感染から保護するGardasilの能力が確認されました。研究はまた、ワクチンが9歳から15歳までの少女と少年のHPVに対する十分な量の抗体の産生を刺激することを示しました。
ガーダシルに関連するリスクは何ですか?
研究(10人に1人以上の患者)でGardasilに関連して最も頻繁に観察される副作用は、発熱(発熱)と注射部位反応(発赤、痛み、腫れ)です。Gardasilで検出された副作用の完全なリストについては、パッケージリーフレットを参照してください
ガーダシルは、有効成分または他の成分のいずれかに過敏(アレルギー)がある可能性のある人には使用しないでください。ガーダシルの1回の投与後にアレルギーの兆候が発生した場合は、他の投与のワクチンの投与を中止する必要があります。高熱の患者の場合、予防接種は延期されるべきです。
ガーダシルが承認されたのはなぜですか?
CHMPは、Gardasilの利点はそのリスクよりも大きいと判断し、医薬品の販売承認を与えることを推奨しました。
ガーダシルに関するその他の情報:
2006年9月20日、欧州委員会はSanofi Pasteur MSDSNCにGardasilの「販売承認」を付与しました。これは欧州連合全体で有効です。
ガーダシル療法の詳細については、添付文書(EPARに含まれています)を読むか、医師または薬剤師に連絡してください。
この要約の最終更新日:2010年7月。
このページで公開されているGardasil-HumanPapillomavirus Vaccineに関する情報は、古くなっているか、不完全である可能性があります。この情報の正しい使用法については、免責事項と有用な情報のページを参照してください。








-cause-sintomi-e-cura.jpg)